En Çok Okunanlar
Özet
Amaç: Seftriakson ve metronidazol kombinasyonu (SEF/MET), intra-abdominal infeksiyon (İAİ)’ların ampirik tedavisinde yaygın olarak kullanılmaktadır. Çalışmada ampirik SEF/MET tedavisi başlanan hastalarda tedavi yanıtı değerlendirilerek, İAİ’ler için güncel tedavi verilerine katkı sağlanılması amaçlandı.
Yöntemler: 2016-2018 arası üç yıllık dönemde, genel cerrahi servisinde parenteral antibiyotik tedavisi alan hastalar geriye dönük olarak incelendi. Çalışmaya İAİ tanısıyla 24 saatten daha uzun süre SEF/MET tedavisi alan 18 yaş ve üzeri hastalar dahil edildi. Hasta özellikleri, son üç ayda antibiyotik kullanımı ve/veya cerrahi girişim öyküsü, infeksiyon kaynağı, cerrahi girişim gereksinimi, klinik ve laboratuvar verileri değerlendirildi. Tedavi değişikliği yapılan ve yapılmayan hasta gruplarında tedavi yanıtı analiz edildi.
Bulgular: Toplam 10 649 hasta değerlendirilmiş olup 591 (%5.5) hasta SEF/MET tedavisi almıştı. Bu hastaların 297 (%50.2)’si çalışma kriterlerini karşılamaktaydı. Hastaların 243 (%81.8)’ünün sadece SEF/MET tedavisi (Grup 1), 54 (%18.2)’ünün ise ek antibiyotik tedavisi aldığı (ortanca 5.gün) saptandı (Grup 2). Malignite varlığı, son üç ayda antibiyotik kullanımı ve cerrahi girişim öyküsü ile tedavi değişikliği arasında istatistiksel olarak anlamlı düzeyde bir ilişki saptandı (p=0.001). Tüm hastaların %75.1’inde infeksiyon odağı safra kesesi (%63) ve biliopankreatik traktustaydı (%12.1). Tedavi değişikliği, İAİ odağı safra kesesi olanların %9.6’sında, biliopankreatik traktus olanların %55.6’sında yapıldı (p=0.001). Tedavi değişikliği yapılanlarda hastane yatış süresi daha uzun ve mortalite daha yüksekti (p=0.001).
Sonuç: İntra-abdominal infeksiyonların odağı safra kesesi olan hastalarda ampirik SEF/MET başlanması uygun olup her beş hastanın dördünde tedaviye yanıt alınmıştı. Ancak odağı biliopankreatik traktus olan, son üç ayda antibiyotik kullanımı, malignitesi veya cerrahi girişim öyküsü olan hastalarda kaynak kontrolü sağlanmasına rağmen SEF/MET tedavisinin yetersiz olduğu görüldü. Bu nedenle infeksiyon kaynağı ve hasta özelliklerinin öğrenilmesi, ampirik tedavide seçilecek antibiyotiğin belirlenmesine katkı sağlayarak tedavi başarısını artıracak, hastanede yatış süresini kısaltacak ve mortaliteyi düşürecektir.
GİRİŞ
İntra-abdominal infeksiyon (İAİ)’lar ile ilgili farklı ülkelerden pek çok dernek (Amerika İnfeksiyon Hastalıkları Derneği, Cerrahi İnfeksiyon Derneği, Dünya Acil Cerrahi Derneği, Alman Gastroenteroloji Derneği, Fransız Anestezi ve Resüsitasyon Derneği, Kanada Tıbbi Mikrobiyoloji ve İnfeksiyon Hastalıkları Derneği, vb.) ve farklı kliniklerin (yoğun bakım, genel cerrahi, infeksiyon hastalıkları ve klinik mikrobiyoloji (İHKM), gastroenteroloji, vb.) uzmanları tarafından kılavuzlar hazırlanmıştır (1-10). Ülkemizde de farklı uzmanlık alanlarından kişilerle hazırlanan ilk uzlaşı raporu 2016 yılında iki farklı dilde yayımlanmıştır (11,12). Tüm kılavuzlarda ve uzlaşı raporlarında; medikal tedavide üçüncü kuşak sefalosporinlerden seftriakson ve metronidazol kombinasyonu (SEF/MET) tedavi önerileri arasında yer alır. Ancak dünya genelinde antibiyotiğe dirençli mikroorganizmaların artması, İAİ’de uygun ampirik tedavi seçiminin gözden geçirilmesini gerektirmektedir (4). Ülkemizde yapılan ve altı merkezin verilerinin değerlendirildiği çalışmada, İAİ’lerde en sık saptanan etken Escherichia coli olup genişlemiş spektrumlu β-laktamaz (GSBL) oranının %29.2-52.5 olduğu bildirilmiştir (13).
Merkezimizden 2020 yılında yapılan bir çalışmada ise toplumdan edinilmiş İAİ olgularında Gram-negatif patojenlerde GSBL oranının %12.3 olduğu gösterilmiştir (14). Bu direnç tipi İAİ’ler için en önemli problemdir (4). Kılavuzlar direnç oranlarına ek olarak antibiyotik seçiminde İAİ’nin kaynağı ve konağın özelliklerinin de dikkate alınması gerektiğini bildirse de halen merkezimizde İAİ’den şüphelenildiğinde SEF/MET ile ampirik antimikrobiyal tedavi başlanmaktadır (10). Bu çalışmada SEF/MET ampirik tedavisinin sık kullanılması nedeniyle; hasta özellikleri, infeksiyon kaynağı ve cerrahi girişim gereksinimi bazında tedaviye yanıtın değişip değişmediğinin belirlenmesi ve İAİ güncel tedavi kılavuzu çalışmalarına katkı sağlanması amaçlandı.
YÖNTEMLER
Bu retrospektif kesitsel çalışma, 2016-2018 arasını kapsayan üç yıllık dönemde, genel cerrahi servisinde parenteral antibiyotik tedavisi alan hastaların verileri ile gerçekleştirildi; veriler hastane bilgi yönetim sisteminden elde edildi. Doksan yataklı servis, yıllık ortalama 2750 ameliyat gerçekleştirilen 1100 yataklı bir üniversite hastanesinde idi. Söz konusu serviste meme-tiroid cerrahisi, üst gastrointestinal sistem, kolorektal ve hepatobiliyer sistem hastalıklarının izleminde farklı ekipler çalışmakta olup karaciğer ve böbrek nakli de yapılmaktadır. Cerrahi ekipler primer olarak; İAİ ön tanılı hastalar için genellikle ampirik SEF/MET veya piperasilin tazobaktam tedavisi başladıktan sonra İHKM konsültasyonu istemektedir.
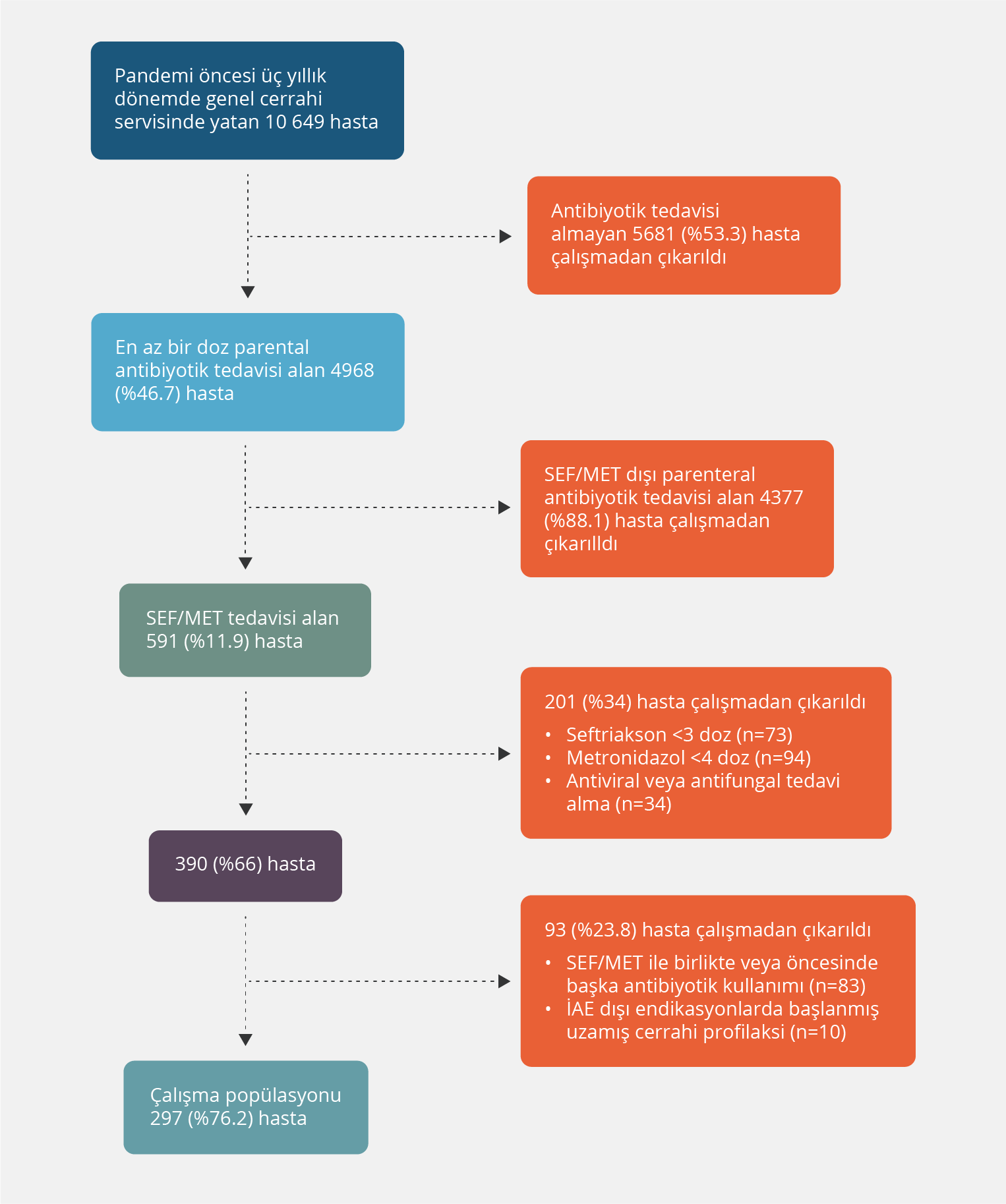
Çalışmaya, İAİ tanısıyla SEF/MET tedavisi başlanan 18 yaş ve üstü hastalar dahil edildi. SEF/MET tedavisi öncesinde veya beraberinde başka bir antibiyotik ve/veya antifungal ve/veya antiviral kullanan hastalar ile üç dozdan az seftriakson, dört dozdan az metronidazol kullanan hastalar çalışma dışında bırakıldı. Ayrıca farklı indikasyonlarda (pnömoni, üriner sistem infeksiyonu, vb.) ve profilaksi amacıyla iki günden uzun süre SEF/MET tedavisi alan hastalar çalışmaya dahil edilmedi (Şekil 1).
Hastaların demografik verileri (yaş, cinsiyet), altta yatan kronik hastalıkları (hipertansiyon, diyabet, kardiyovasküler hastalık, kronik akciğer hastalıkları, kronik böbrek hastalıkları ve malignite), hastane yatışı öncesi son üç ayda antibiyotik kullanımı ve son üç aydaki cerrahi girişim bilgileri kaydedildi. Hastaların izleminde tedavinin 0. gün, 48-72. saat, 5-7. gün ve ek olarak tedavi değişikliğinin uygulandığı günlerdeki klinik (vücut sıcaklığı, kan basıncı, kardiyak atım sayısı) ve laboratuvar [beyaz küre sayısı, hemoglobin ve albümin düzeyi, C-reaktif protein (CRP) değerleri, kültür sonuçları] bulguları, cerrahi girişimleri, tedavi süreleri, hastane yatış süreleri ve hasta sonlanımları hasta kayıt dosyalarından elde edildi.
İntra-abdominal infeksiyon lokalizasyonu; safra kesesi, biliopankreatik traktus, apendiks, üst gastrointestinal sistem (Üst GİS), kolon ve diğer odaklar (peritonit, batın içi apse vb.) şeklinde altı gruba ayrıldı.
Girişimsel işlemler; ameliyat (laparatomi ve laparoskopi) ve perkütan drenaj-ERCP (Endoskopik Retrograd Kolanjiyo Pankreatografi) olarak gruplandırıldı.
Hastalar izlem için; medikal tedavi değişikliğine göre ve kaynak kontrolü sağlamaya yönelik uygulanan cerrahi girişim ile tedavi değişikliği ilişkisine göre aşağıda verilen gruplara ayrıldı.
Medikal tedavi değişikliğine göre;
Grup 1: Sadece SEF/MET kullanan ve ek antibiyotik kullanmayan hastalar.
Grup 2: SEF/MET tedavisine ek antibiyotik alan hastalar.
Cerrahi girişim ile tedavi değişikliği ilişkisini araştırmak için;
A Grubu: Cerrahi girişim yapılmaksızın SEF/MET tedavisinin yeterli olduğu hastalar.
B Grubu: SEF/MET tedavisine rağmen kaynak kontrolü sağlanması gereken hastalar.
C Grubu: Tedavi revizyonuna rağmen kaynak kontrolünün sağlanması gereken hastalar.
D Grubu: Cerrahi girişim yapılmaksızın sadece tedavi revizyonu yapılan hastalar.
Çalışma için Dokuz Eylül Üniversitesi Girişimsel Olmayan Araştırmalar Etik Kurulu’ndan 08 Mayıs 2019 tarih ve 2019/12-08 karar numarası ile onay alındı.
İstatistiksel Analizler
Tanımlayıcı analiz olarak; sayım tipi değişkenlerin sayı ve yüzde değerleri, ölçüm tipi değişkenlerin ortalama, standart sapma, ortanca, minimum-maksimum ve aralık değerleri sunuldu. Sayım tipi değişkenler için Pearson’s χ², ölçüm tipi değişkenlerin karşılaştırmasında parametrik test koşullarını sağlama durumuna göre Student T testi ya da Mann-Whitney U testi kullanıldı. Verilerin analizi, “Statistical Package for the Social Sciences” (SPSS) versiyon 24.0 programı (IBM Corp., Armonk, NY, ABD) ile yapıldı. İstatistiksel olarak anlamlılık düzeyi p<0.05 olarak belirlendi.
BULGULAR
Toplam 10 649 hasta değerlendirilmiş olup 4968 (%46.7) hastanın en az bir doz parenteral antibiyotik tedavisi aldığı ve 591 (%11.9) hastanın ise SEF/MET tedavisi aldığı tespit edildi. SEF/MET tedavisi alan hastalar çalışmanın dahil edilme kriterlerine uygun olarak değerlendirildi ve İAİ tanısı ile ampirik SEF/MET başlanan 297 (%50.2) hasta çalışmaya dahil edildi.
Sadece SEF/MET ile tedavi edilen ve başka ek antibiyotik almayan hasta sayısı 243 (%81.8) idi (Grup 1); 54 (%18.2) hastada ise ortanca 5. (minimum=2, maksimum=25) günde SEF/MET tedavisi yetersiz kalmış ve ek antibiyotik ihtiyacı gelişmişti (Grup 2). Üç haftanın üzerinde SEF/MET tedavisi alan tek bir hasta vardı; klatskin tümörüne sekonder kolesistit nedeniyle SEF/MET tedavisi başlanmıştı. Hastanın tedavisinin 10. gününde perkütan biliyer drenaj ile kaynak kontrolü sağlamaya yönelik girişim uygulanmış ve tedavisine devam edilmişti. Ancak SEF/MET tedavisinin 25. gününde hastada ateş yüksekliği saptanması nedeniyle tedavisi revize edilmişti.
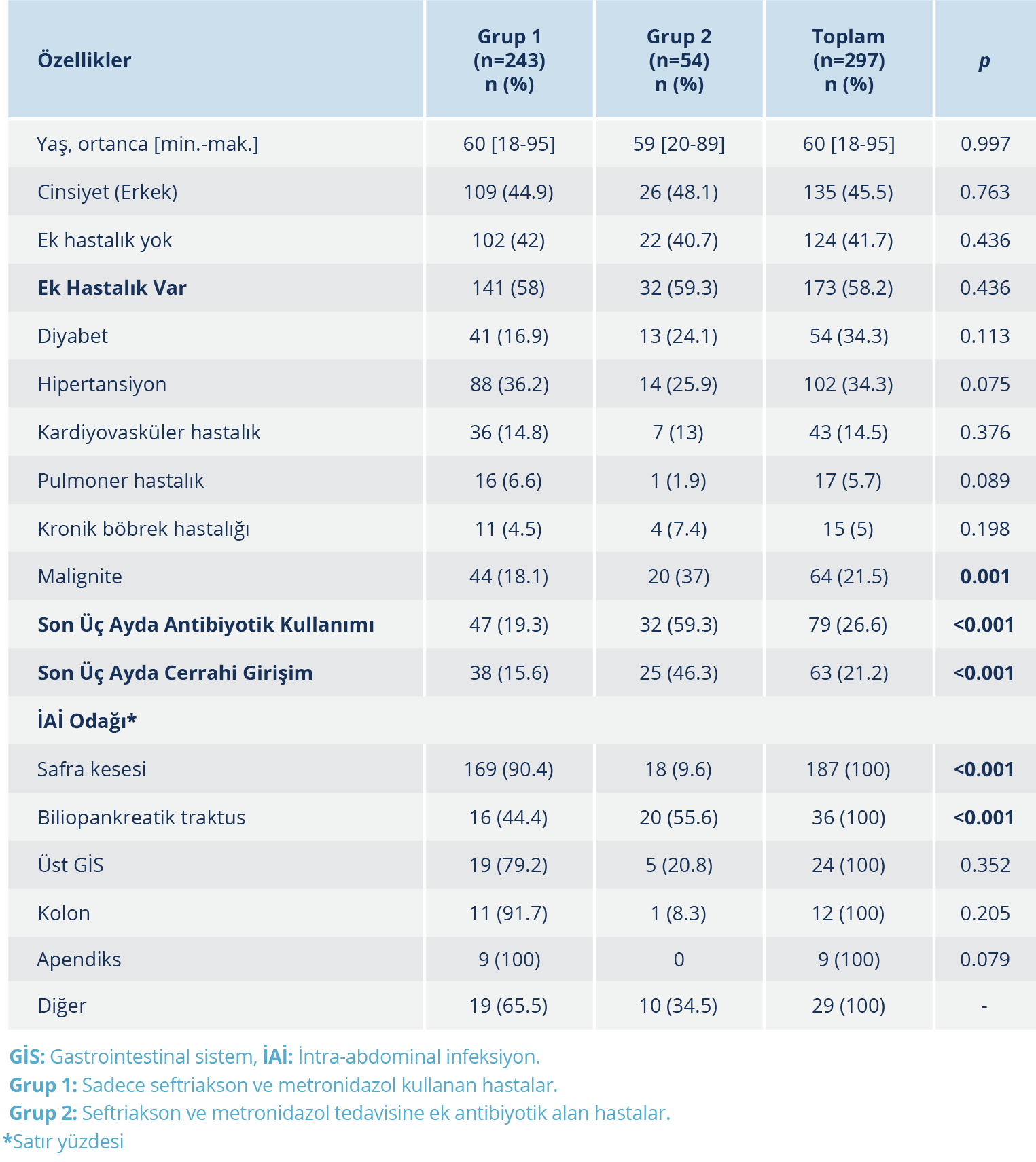
Her iki grupta yaş ortalaması ve cinsiyet dağılımı benzerdi. Malignite varlığı, son üç ayda antibiyotik kullanımı ve son üç ayda cerrahi girişim öyküsü ile tedavi değişikliği gerekliliği arasında istatistiksel olarak anlamlı düzeyde bir ilişki saptandı. Hastaların %31.6 (94/297)’sının malignite dahil herhangi bir ek hastalığı, son üç ayda antibiyotik kullanımı ve cerrahi girişim öyküsü yoktu. Bu hastaların sadece %7.4 (7/94)’ünde ek antibiyotik ihtiyacı gelişmişti.
Hastaların tamamının %75.1 (223/297)’inde infeksiyon odağı safra kesesi (n=187, %63) ve biliopankreatik traktustaydı (n=36, %12.1). İntra-abdominal infeksiyon odağı safra kesesi olan hastaların %9.6 (18/187)’sında ek antibiyotik ihtiyacı gelişirken, infeksiyon odağı biliopankreatik traktus olan hastaların %55.6 (20/36)’sında ek antibiyotik ihtiyacı gelişmişti. İnfeksiyon odağı açısından gruplar arasında istatistiksel olarak anlamlı düzeyde farklılık saptandı (p=0.001). Hasta özellikleri ve risk faktörleri Tablo 1’de verildi.
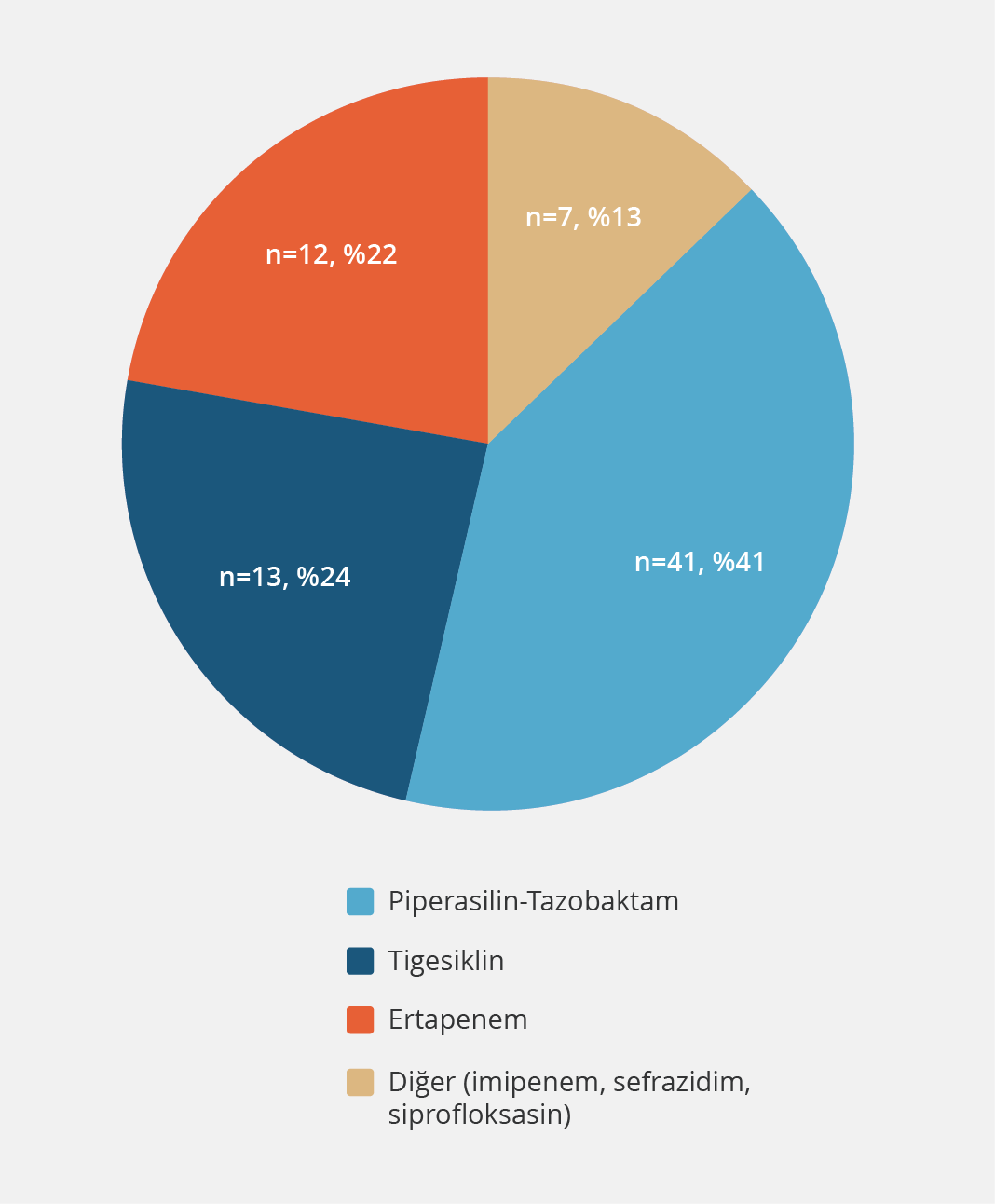
Grup 2’deki hastaların 46 (%85.2)’sında tedavi değişikliği ampirikti; hastaların 18 (%33.3)’inde klinik ve laboratuvar, 17 (%31.5)’sinde klinik, 11 (%20.4)’inde ise laboratuvar sonuçları değerlendirilerek tedavi değiştirilmişti. Hastaların 8 (%14.8)’inde ise kültür sonuçları ile etkene yönelik tedavi değişikliği yapılmıştı. SEF/MET tedavisi sonrasında kullanılan antibiyotiklerin dağılımı Şekil 2’de verildi. Tedavi değişikliğinin hastaların 41 (%75.9)’inde İHKM konsültasyonu sonucuna göre, 13 (%24.1)’ünde ise primer hekimi tarafından değerlendirilerek uygulandığı görüldü.
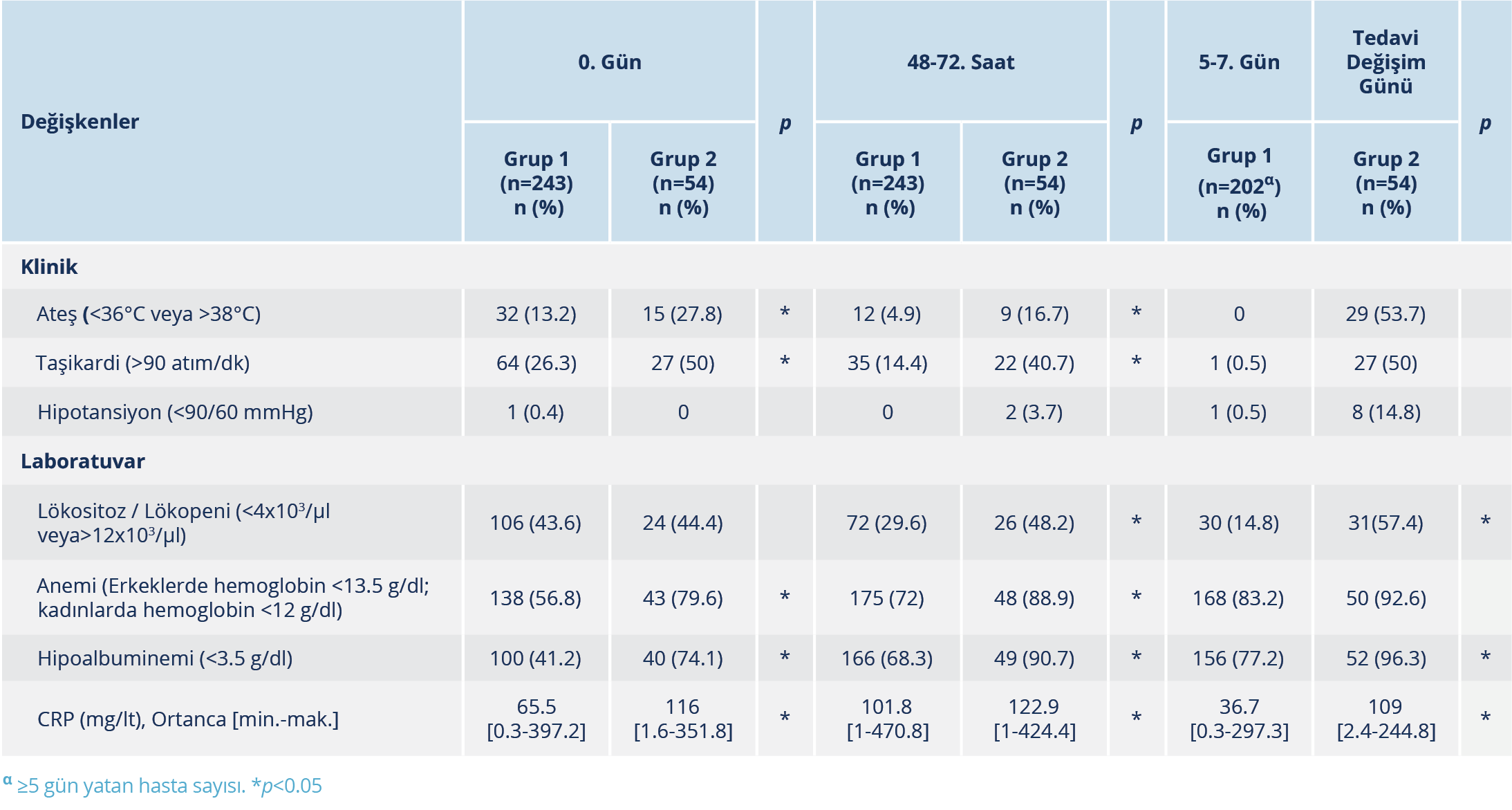
SEF/MET tedavisinin başlangıcında Grup 1 ve Grup 2’de lökositoz oranları benzerken; ateş yüksekliği, taşikardi, anemi ve hipoalbüminemi varlığı Grup 2’deki hastalarda daha sıktı ve ortalama CRP değerleri yaklaşık iki kat daha yüksekti. Tedavinin 48-72. saatinde ise tüm klinik ve laboratuvar verileri açısından iki grup arasında istatistiksel farklılık olduğu görüldü. SEF/MET tedavisinin 5-7. gününde Grup 1’deki hastaların sadece birinde taşikardi ve hipotansiyon saptanırken, Grup 2’deki hastaların yaklaşık yarısında tedavi revizyonu yapıldığı günde ateş yüksekliği ve taşikardi kliniği mevcuttu. SEF/MET tedavisinin izlemindeki klinik ve laboratuvar verileri Tablo 2’de verildi.
SEF/MET tedavisi alan Grup 1’deki hastaların ortanca 7 (minimum=2, maksimum=60) gün, ek antibiyotik ihtiyacı gelişen Grup 2’deki hastaların ise ortanca 22 (minimum=7, maksimum=88) gün hastanede yattığı saptandı; gruplar arasındaki bu farklılık istatistiksel olarak anlamlıydı (p=0.001). Grup 2’deki hastaların 11 (%20.4)’inde 30 gün içinde mortalite saptanırken, Grup 1’deki hastaların ise sadece 6 (%2.5)’sında 30 gün içinde mortalite saptandı ve bu fark istatistiksel olarak anlamlıydı (p=0.001).
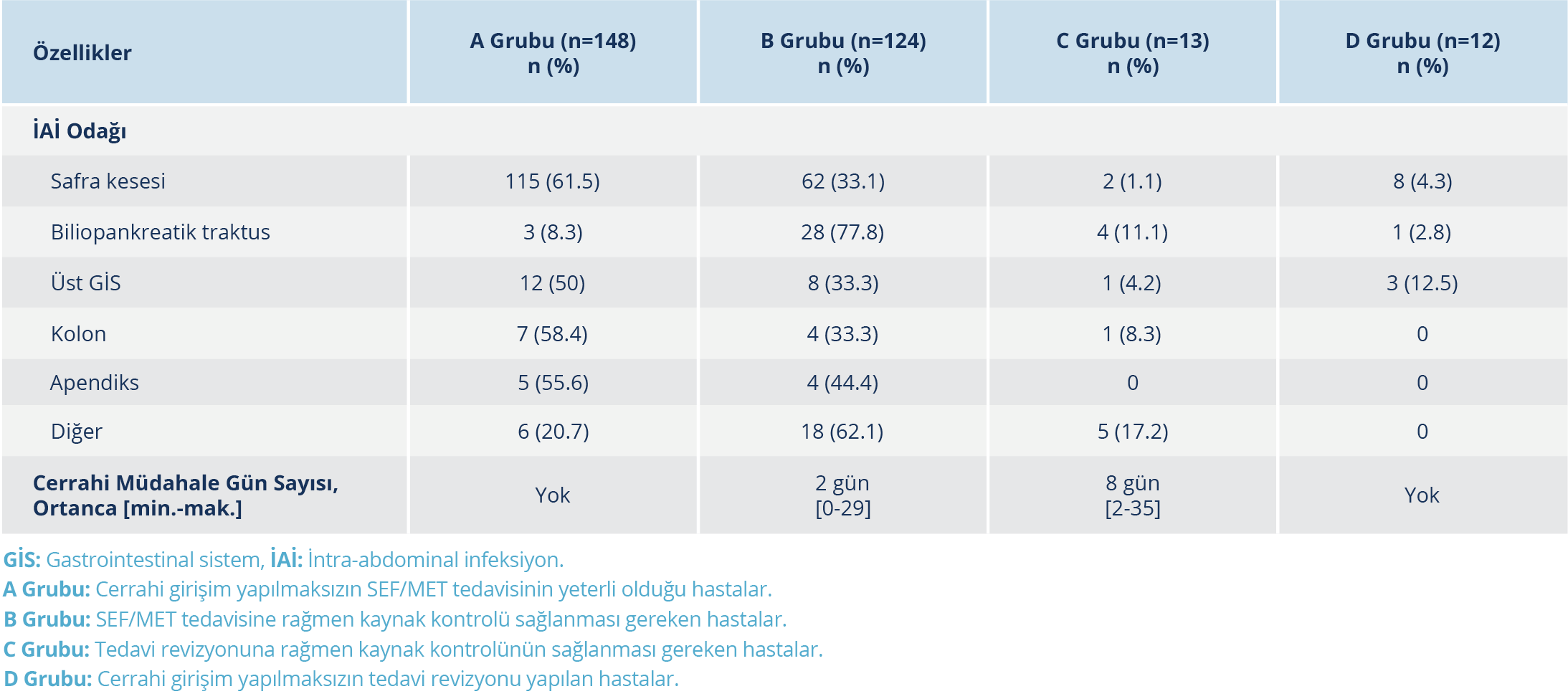
Kaynak kontrolünü sağlamaya yönelik uygulanan cerrahi girişim ile tedavi değişikliği ilişkisini araştırmak için dört alt grup oluşturuldu ve İAİ odaklarına göre incelendi (Tablo 3). Buna göre tüm hastaların %49.8 (148/297)’inde cerrahi girişim yapılmaksızın SEF/MET tedavisi yeterli olurken (A grubu), %41.8 (124/297)’inde SEF/MET tedavisine rağmen kaynak kontrolü sağlanması gerekti (B grubu). Hastaların %4.4 (13/297)’ünde SEF/MET tedavisi değiştirilmesine rağmen cerrahi girişim gerektiği (C grubu), %4 (12/297)’ünde ise cerrahi girişim uygulanmaksızın sadece SEF/MET tedavisinde değişiklik yapıldığı görüldü (D grubu). Gruplar, İAİ odaklarına göre değerlendirildiğinde infeksiyon kaynağı safra kesesi olan hastaların %61.5 (115/187)’inde cerrahi girişim yapılmaksızın SEF/MET tedavisi tek başına yeterli olurken, infeksiyon kaynağı biliopankreatik traktus olan hastalarda bu oranın %8.3 (3/36) olduğu görüldü. Biliopankreatik traktusta tedaviden bağımsız olarak hastaların %88.9 (32/36)’unda kaynak kontrolünü sağlamaya yönelik cerrahi girişim uygulanmıştı.
Hastaların %46 (137/297)’sında kaynak kontrolünü sağlamaya yönelik cerrahi girişim uygulandığı görüldü (B ve C grubu). İnvazif işlem yapılan 80 (%58.4) hastada perkütan drenaj-ERCP girişimsel işleminin yapıldığı ve bu hastaların 68 (%85.1)’inde infeksiyon odağının safra kesesi (n=43, %53.8) ve biliopankreatik traktus (n=25, %31.3) olduğu saptandı.
Kaynak kontrolüne yönelik girişim yapılan hastaların (B ve C grubu) sadece %16 (22/137)’sında girişim esnasında kültür örneği alındığı ve bu örneklerin %63.6 (14/22)’sında üreme saptandığı görüldü. Örneklerin 17 (%77.3)’sinin perkütan drenaj-ERCP işlemleri sırasında alındığı ve bu örneklerin %76.5 (13/17)’inde üreme saptandığı, beş örneğin ise ameliyat esnasında elde edildiği ve sadece 1 (%20)’inde üreme saptandığı belirlendi. Kaynak kontrolüne yönelik girişim yapılarak örnek alınan ve üreme saptanmış olan 14 örneğin 9 (%40.9)’unda SEF/MET tedavisine dirençli veya etki spektrumu dışında etkenlerin üremiş olduğu görüldü. Üreme saptanan 14 örneğin 5 (%35.8)’inde E. coli, 3 (%21.4)’ünde Enterococcus spp., 1 (%7.1)’inde Klebsiella pneumoniae, 1 (%7.1)’inde Enterobacter cloacae ve 4 (%28.6)’ünde polimikrobiyal üreme tespit edildi.
İRDELEME
İntra-abdominal infeksiyon nedeniyle izlenen tüm olgularda ampirik olarak başlanmış olan SEF/MET tedavisi, uygun kaynak kontrolü sağlandığı durumlarda hastaların %81.8’inde tedavi revizyonu gerektirmemiş ve başarılı olmuştu. Ancak infeksiyon odağı biliopankreatik traktusta olan veya son üç ayda antibiyotik kullanımı öyküsü, eşlik eden malignitesi veya cerrahi girişim öyküsü olan hastalarda SEF/MET tedavisi, uygun kaynak kontrolü sağlanmasına rağmen yetersiz kalabilmekteydi. Bu hastalarda yakın klinik ve laboratuvar izlemiyle birlikte kaynak kontrolüne yönelik yapılan invazif girişimlerde alınan kültür örneği sonuçlarına göre etkene yönelik tedavi başlanması mortalite ve morbiditeyi azaltacaktır.
Çalışma grupları İAİ kaynağı açısından değerlendirildiğinde en sık karşılaşılan odak safra kesesi ve biliopankreatik traktus idi. Diğer infeksiyon odaklarında, ampirik tedavide SEF/MET dışı antibiyotiklerin tercih edilmiş olması veya SEF/MET tedavisinin cerrahi profilaksi amacıyla uygulanmış olması bu hastaların çalışma dışında kalmalarına neden oldu.
İntra-abdominal infeksiyon hastalarında yapılan çalışmalarda, biliopankreatik traktus ve safra kesesi ayrımı yapılmamıştır (15-18). Çalışmamızda safra kesesi ve biliopankreatik traktus infeksiyon odağı ayrı olarak değerlendirilmiş olup SEF/MET tedavisi safra kesesi kaynaklı infeksiyonların tedavisinde yeterli olurken biliopankreatik traktus kaynaklı infeksiyonlarda SEF/MET tedavisinin yetersiz kalabildiği ve daha sık kaynak kontrolü sağlanması gerektiği görüldü. Bu durum biliopankreatik traktusta infeksiyonu olan hastaların yarısından fazlasında traktusun drenajını bozan taş veya malignite varlığı, son üç ayda antibiyotik kullanımı veya cerrahi girişim öyküsü olması ile açıklanabilir. Bu risk faktörlerine sahip hastaların ampirik tedavi seçiminde, SEF/MET tedavisine dirençli veya etki spektrumu dışındaki etkenler de göz önünde bulundurulmalıdır.
Ülkemizde yapılan bir çalışmada, beş ay süresince genel cerrahi doktorları tarafından acil olarak ameliyat edilen 233 toplum kökenli İAİ olgusunun (56’sı komplike İAİ olarak tanı almış) sadece 12 (%5.1)’sinden kültür alındığı ve bu kültürlerin altısında üreme olduğu ve üreyen etkenlerin üçünde seftriaksona direnç saptandığı bildirilmiştir (12). Benzer olarak çalışmamızda da sadece 22 (%16) hastada girişimsel işlem sırasında kültür örneği alındığı, alınan örneklerin 14 (%63.6)’ünde üreme saptandığı, 9 (%40.9)’unda SEF/MET tedavisine dirençli veya etki spektrumu dışında etkenlerin ürediği görüldü. Kültür alınan ve üreme olanların %28.6’sında polimikrobiyal üreme saptanmıştı. Antibiyotik direncindeki artış göz önüne alındığında, İAİ hastalarında kaynak kontrolünün sağlanmasına yönelik yapılan tüm girişimsel işlemlerde örnek alınması teşvik edilerek, üreyen etken ve duyarlılık verileri ile yerel tedavi protokollerinin oluşturulmasına katkı sağlanabilir. Bu durum İAİ hastalarında metronidazolün de indikasyonunun belirlenmesini sorgulatacaktır.
Tedavi revizyonu yapılan hastalarda çoğunlukla piperasilin-tazobaktam, tigesiklin ve ertapenem tedavileri kullanılmış olup ulusal ve uluslararası birçok çalışmada önerilen antibiyotikler ile uyumluydu (12,17,18). Kültür sonuçlarında en sık üreyen etken E. coli (5/14) idi. Üreyen etkenler ve oranları Tan ve arkadaşları (15) tarafından yapılan çalışma ile uyumluydu.
Çalışmanın tek merkezde yürütülmüş olup hasta verilerinin retrospektif olarak değerlendirilmesi en önemli kısıtlılıktır. Çalışma popülasyonu seçilirken en az 48 saat antibiyotik kullanımı kriter olarak alınsa da ampirik antibiyotik kullanımının indikasyonlarının sorgulanamaması, tedavi değişikliği için belirlenmiş kriterlerin olmaması, tedavi değişikliği yapılan hasta grubunun sayısal olarak az olması, hastaların infeksiyon odağı açısından safra kesesi ve biliopankreatik traktusta yoğunlaşması ve diğer odaklardaki hasta sayılarının nispeten az olması çalışmamızın diğer kısıtlılıklarıdır. Daha fazla hasta örneğinin incelendiği çok merkezli randomize kontrollü çalışmalara ihtiyaç vardır.
Ampirik antibiyotik tedavisine başlanırken hasta özellikleri, olası İAİ odağı ve cerrahi girişim gerekliliği sorgulanmalıdır. SEF/MET tedavisi, özellikle İAİ odağı safra kesesi olan hastalarda ampirik tedavide tercih edilebilir. Ancak odağı biliopankreatik traktus olan, son üç ayda antibiyotik kullanımı, malignitesi veya cerrahi girişim öyküsü olan hastalarda kaynak kontrolü sağlanmasına rağmen SEF/MET tedavisi yetersiz kalabilmektedir. Bu durumda kaynak kontrolü açısından hasta tekrar değerlendirilmeli, mutlaka kültür alınarak etken izole edilmeye çalışılmalıdır. Sonuç olarak; değişikliğe ihtiyaç duyulmayacak ampirik tedaviler ile hastanede yatış süresi kısalacak ve mortalite düşecektir.
Hasta Onamı
Veriler retrospektif olarak incelendiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma için Dokuz Eylül Üniversitesi Girişimsel Olmayan Araştırmalar Etik Kurulu’ndan 08 Mayıs 2019 tarih ve 2019/12-08 karar numarası ile onay alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram – V.A.O., Z.S.D.; Tasarım – V.A.O., Z.S.D., Ç.I.; Denetleme – V.A.O., Z.S.D.; Kaynak ve Fon Sağlama – V.A.O., Z.S.D.; Malzemeler/Hastalar – V.A.O., Ç.I.; Veri Toplama ve/veya İşleme – Z.S.D., Ç.I.; Analiz ve/veya Yorum – Z.S.D., Ç.I., V.A.O.; Literatür Taraması – Ç.I., V.A.O.; Makale Yazımı – Z.S.D., V.A.O., Ç.I.; Eleştirel İnceleme – Z.S.D., V.A.O., Ç.I.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Bilimsel Etkinlik
9-12 Mart 2022 tarihinde gerçekleştirilen 22. Uluslararası Türk Klinik Mikrobiyoloji ve İnfeksiyon Hastalıkları Kongresi’nde poster olarak sunulmuştur.
Referanslar
- Lopez N, Kobayashi L, Coimbra R. A Comprehensive review of abdominal infections. World J Emerg Surg. 2011;6:7. [CrossRef]
- Solomkin JS, Mazuski JE, Bradley JS, et al. Diagnosis and management of complicated intra-abdominal infection in adults and children: guidelines by the Surgical Infection Society and the Infectious Diseases Society of America. Clin Infect Dis. 2010;50(2):133-64. Erratum in: Clin Infect Dis. 2010;50(12):1695. [CrossRef]
- Chow AW, Evans GA, Nathens AB, et al. Canadian practice guidelines for surgical intra-abdominal infections. Can J Infect Dis Med Microbiol. 2010;21(1):11-37. [CrossRef]
- Sartelli M, Coccolini F, Kluger Y, et al. WSES/GAIS/SIS-E/WSIS/AAST global clinical pathways for patients with intra-abdominal infections. World J Emerg Surg. 2021;16(1):49. [CrossRef]
- Montravers P, Dupont H, Leone M, et al. Guidelines for management of intra-abdominal infections. Anaesth Crit Care Pain Med. 2015;34(2):117-30. [CrossRef]
- Kruis W, Germer CT, Leifeld L; German Society for Gastroenterology, Digestive and Metabolic Diseases and The German Society for General and Visceral Surgery. Diverticular disease: Guidelines of the German society for gastroenterology, digestive and metabolic diseases and the German society for general and visceral surgery. Digestion. 2014;90(3):190-207. [CrossRef]
- Bassetti M, Marchetti M, Chakrabarti A, et al. A research agenda on the management of intra-abdominal candidiasis: Results from a consensus of multinational experts. Intensive Care Med. 2013;39(12):2092-106. [CrossRef]
- Solomkin JS, Mazuski JE, Baron EJ, et al; Infectious Diseases Society of America. Guidelines for the selection of anti-infective agents for complicated intra-abdominal infections. Clin Infect Dis. 2003;37(8):997-1005. [CrossRef]
- Tenner S, Baillie J, DeWitt J, Vege SS; American College of Gastroenterology. American College of Gastroenterology guideline: management of acute pancreatitis. Am J Gastroenterol. 2013;108(9):1400-16. Erratum in: Am J Gastroenterol. 2014;109(2):302. [CrossRef]
- Mazuski JE, Tessier JM, May AK, et al. The Surgical Infection Society Revised Guidelines on the Management of Intra-Abdominal Infection. Surg Infect (Larchmt). 2017;18(1):1-76. [CrossRef]
- İntra-abdominal İnfeksiyonlar İçin Öneriler “Uzlaşı Raporu” [Internet]. Türkiye Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Uzmanlık Derneği (EKMUD), Türk Hastane İnfeksiyonları ve Kontrolü Derneği, Türk Cerrahi Derneği, Türk Kolon ve Rektum Cerrahisi Derneği, Fıtık Derneği ve Türk Hepato Pankreato Bilier Cerrahi Derneği. [erişim 20 Eylül 2023]. https://www.turkcer.org.tr/files/files/intraabdominal_kilavuz.pdf
- Avkan-Oğuz V, Baykam N, Sökmen S, et al. Recommendations for intra-abdominal infections consensus report. Ulus Cerrahi Derg. 2016;32(4):306-21. [CrossRef]
- Koksal I, Yilmaz G, Unal S, et al. Epidemiology and susceptibility of pathogens from SMART 2011-12 Turkey: evaluation of hospital-acquired versus community-acquired urinary tract infections and ICU- versus non-ICU-associated intra-abdominal infections. J Antimicrob Chemother. 2017;72(5):1364-72. [CrossRef]
- Avkan-Oğuz V, Baykam N, Korten V, et al. Antimicrobial resistance and molecular patterns in community-acquired complicated intra-abdominal infections: A multicentric study. Infect Dis Clin Microbiol. 2020;2:71-7. [CrossRef]
- Tan A, Rouse M, Kew N, Qin S, La Paglia D, Pham T. The appropriateness of ceftriaxone and metronidazole as empirical therapy in managing complicated intra-abdominal infection-experience from Western Health, Australia. PeerJ. 2018;6:e5383. [CrossRef]
- Solomkin J, Zhao YP, Ma EL, Chen MJ, Hampel B; DRAGON Study Team. Moxifloxacin is non-inferior to combination therapy with ceftriaxone plus metronidazole in patients with community-origin complicated intra-abdominal infections. Int J Antimicrob Agents. 2009;34(5):439-45. [CrossRef]
- Navarro NS Jr, Campos MI, Alvarado R, et al; Oasis II Study Team. Ertapenem versus ceftriaxone and metronidazole as treatment for complicated intra-abdominal infections. Int J Surg. 2005;3(1):25-34. [CrossRef]
- Qvist N, Warren B, Leister-Tebbe H, et al. Efficacy of tigecycline versus ceftriaxone plus metronidazole for the treatment of complicated intra-abdominal infections: Results from a randomized, controlled trial. Surg Infect (Larchmt). 2012;13(2):102-9. [CrossRef]