En Çok Okunanlar
Özet
Amaç: Tüberküloz (TB), tüm dünyada morbidite ve mortalitenin önde gelen nedenlerinden biridir. Basit, hızlı ve aynı zamanda doğru tanı testlerinin olmaması nedeniyle TB’nin kontrolü güçleşmektedir. Dünya Sağlık Örgütü›nün yeni TB kontrol stratejisinde moleküler tanı teknikleri büyük önem taşımaktadır. Çalışmamızın amacı M. Tuberculosis’in ve rifampisin (RİF) direncinin doğrudan tespiti için kullanılan GeneXpert MTB/RIF testinin performansının değerlendirilmesi ve altın standart olan kültür yöntemleriyle karşılaştırılmasıdır.
Yöntemler: Çalışmamızda 2020 yılı boyunca laboratuvarımıza gönderilen pulmoner ve ekstrapulmoner örnekler dahil edildi. Toplam 379 örnek rutin olarak aside dirençli basil varlığı için preparat hazırlanarak incelendi; ardından Löwenstein-Jensen (LJ) ve “Mycobacterium Growth Indicator Tubes” (MGIT) (Becton Dickinson, ABD) ortamında kültürleri yapıldı. Hazırlanan örnekler GeneXpert MTB/RIF testi (Cepheid, ABD) ile çalışıldı. Tüberküloz dışı mikobakteri (TDM) olarak tanımlanan hasta örnekleri için klinik olarak tür tayini istemi olması halinde, “GenoType Mycobacterium CM” test kiti (Hain Lifescience, Almanya) ile çalışıldı. GeneXpert MTB/RIF testinin performansını değerlendirmek için sonuçlar karşılaştırıldı.
Bulgular: Toplam 379 pulmoner ve ekstrapulmoner örneğin 1 (%0.2)’inde yayma sonucu pozitifti; yayma sonucu negatif olan 378 örnekten 21 (%5.5)’inin kültüründe üreme oldu ve hepsinin de GeneXpert MTB/RIF testiyle pozitif olduğu doğrulandı. GeneXpert MTB/RIF test sonucu pozitif olan 22 örnekten 21 (%95.4)’i RİF’e duyarlı, 1 (%4.6)’i ise dirençli idi. BD BACTECTM MGITTM 960 tanımlama sistemi (Becton Dickinson, ABD)’nin sonuçları referans olarak kabul edilerek, mevcut sınırlı verilerle yapılan istatistiksel analizlerde GeneXpert MTB/RIF testinin özgüllüğü %98, duyarlılığı %68, pozitif öngörü değeri %68 ve negatif öngörü değeri %98 olarak hesaplandı.
Sonuç: GeneXpert testi, pulmoner ve ekstrapulmoner örneklerde MTB’nin saptanması için ADB yayma mikroskobuna göre daha yüksek bir duyarlılık gösterdi. Erken tespit, hastalığın bulaşmasının kontrol altına alınmasını ve TB tedavisinin zamanında başlamasını kolaylaştırır. Bu doğrultuda, GeneXpert testinin uygulanması, çoklu ilaç dirençli TB olgularının önemli ölçüde azalmasını sağlayacaktır.
GİRİŞ
Tüberküloz (TB), tüm dünyada önemli bir halk sağlığı sorunu olup morbidite ve mortalitenin en yaygın nedenlerinden biridir; öyle ki tek bir infeksiyondan kaynaklanan ölümlerin önde gelen nedenidir (1). Mycobacterium tuberculosis’in neden olduğu bir infeksiyon olan TB genellikle akciğerleri etkiler; ancak vücudun diğer kısımlarını da etkileyebilir. Pulmoner TB (PTB) aerosoller yoluyla kolaylıkla yayılır (2). Dünya Sağlık Örgütü (DSÖ)’nün 2023 Küresel Tüberküloz Raporu’na göre, COVID-19 pandemisi sonrası tüberkülozun tanımlanması ve yönetimi üzerindeki olumsuz etkilerin azalması nedeniyle, 2022 yılında yeni tüberkülozlu hasta sayısı 7.5 milyona ulaşmıştır. Bu sayı, 2019 yılında 7.1 milyon, 2020 yılında 5.8 milyon ve 2021 yılında 6.4 milyon olarak bildirilmiştir. 2023 yılında tespit edilen hasta sayısı, 1995 yılından beri görülen en yüksek yıllık yeni hasta sayısıdır (3). Türkiye’de Verem Savaşı 2021 Raporu’na göre, 2019 yılında 11 401, 2020 yılında ise 8925 olgu raporlanmıştır (4).
M. tuberculosis’in insandan insana bulaşma riskinin yüksek olması ve çok ilaca dirençli tüberküloz (ÇİD-TB) ile yaygın ilaca dirençli tüberkülozun (YİD-TB) ortaya çıkması, hızlı tespiti ve infekte hastalarda rifampisin (RİF) direncinin belirlenmesini hastalık yönetimi açısından zorunlu hale getirmektedir (5). Tüberküloz tanısında balgam kültürü altın standarttır; ancak bu yöntem, kontaminasyon riski barındırır, yoğun emek gerektirir ve iki ila sekiz hafta kadar sürmesi nedeniyle zaman alır. Bu durum, tedavinin gecikmesine ve bulaşıcılığın artmasına neden olabilir (6).
Erken tanı, TB’nin yönetimi ve kontrolünde son derece önemlidir. Aside dirençli basiller (ADB’ler) için yayma mikroskobisi hızlı ve ucuzdur; bu nedenle özellikle kaynakların kısıtlı olduğu ortamlarda TB teşhisi için hâlâ birinci basamak tanı yöntemi olarak kullanılmaktadır. Ancak yöntemin duyarlılığı (%20-80) değişkendir ve düşük pozitif prediktif değere sahiptir (7). Dolayısıyla, TB yönetiminde alternatif bir hızlı tanı aracı kullanmak vazgeçilmezdir. Erken tedavi, olumlu hasta sonuçları ve daha etkili halk sağlığı müdahaleleri için gerekli olan hızlı tanı yöntemleri, nükleik asit amplifikasyon tekniklerine dayanır (8).
Yüksek TB yükü olan ülkeler, karşı karşıya kaldıkları büyük zorluklar ve ÇİD-TB nedeniyle moleküler testlerin dikkate değer bir şekilde gelişmesine tanık olmuştur (9-12). Nükleik asit amplifikasyon testleri (NAAT’lar), 1996’dan beri hastalarda TB’nin rutin değerlendirmesi için önerilmiş olmakla birlikte yaygın olarak uygulanmamıştır. Aralık 2010’da DSÖ, TB’nin endemik olduğu ülkelerde TB ve TB direncinin teşhisinde kullanılmak üzere yeni bir moleküler test olan GeneXpert MTB/RIF (Cepheid, ABD) testini onaylamıştır. Söz konusu test, hızlı bir antibiyotik duyarlılık testine ek olarak, hızlı TB teşhisi için kartuş tabanlı NAAT’ın uygulandığı otomatik bir tanımlama testidir. M. tuberculosis DNA’sı ve rifampisin direnci (RD), bu testle eş zamanlı olarak belirlenebilir (13). Ayrıca, RD’den sorumlu gen mutasyonunu tanımlayabildiği için TB ve RD’nin daha erken teşhis edilmesine ve uygun bir anti-TB rejiminin zamanında başlatılmasına olanak sağlar (13,14).
Çalışmamızın amacı, M. tuberculosis’in ve RD’nin doğrudan tespiti için kullanılan GeneXpert MTB/RIF testinin performansının değerlendirilmesi ve altın standart olan kültür yöntemleriyle karşılaştırılmasıdır.
YÖNTEMLER
Çalışmaya, 2020 yılı boyunca laboratuvarımıza gönderilen toplam 379 pulmoner ve ekstrapulmoner örnek dahil edildi. Steril olmayan örnekler, dekontaminasyon ve homojenizasyon işlemine tabi tutuldu; bu işlemler için standart N-asetil-L-sistein ve sodyum hidroksit yöntemi kullanıldı. Taze hazırlanmış BD MycoPrepTM NALC-NaOH çözeltisi (Becton Dickinson, ABD) eşit hacimde örneklere ilave edildi, vortekste karıştırıldı ve oda sıcaklığında 15 dakika bekletildi.
Daha sonra karışıma miktarının iki katı steril fosfat tamponu (pH 6.8) (Becton Dickinson, ABD) ilave edilerek, 3000 rpm’de 20 dakika santrifüj edildi. Süpernatan döküldü ve çökeltinin, ileri işlemler için 2.5 ml steril fosfat tamponunda çözünmesi sağlandı. Hazırlanan çözeltiden, aside dirençli basillerin (ADB) varlığını belirlemek amacıyla rutin olarak preparatlar hazırlandı ve mikroskobik inceleme yapıldı. Yaymalar hazırlandı, sabitlendi ve Ziehl-Neelsen boyası (RTA Laboratuvarları, Türkiye) ile boyanarak 100x büyütme altında mikroskopla incelendi (16).
0.5 ml çözünmüş numune, kültür için katı Löwenstein-Jensen (LJ) besiyerine (Becton Dickinson, ABD) ekildi; LJ besiyeri haftalık olarak kontrol edilerek sekiz hafta boyunca 37°C’de inkübe edildi. Sıvı besiyeri olarak ise “Mycobacterium Growth Indicator Tubes” (MGIT) (Becton Dickinson, ABD)’e 0.5 ml numune çözeltisi eklendi ve BD BACTECTM MGITTM 960 tanımlama sistemi (Becton Dickinson, ABD) ile 37°C’de altı hafta süreyle inkübe edildi. İnkübasyon süresinin sonunda üreme gözlenmeyen örnekler çıkarıldı. Üreme gözlenen suşların tanımlamasında, MPT64 proteinini saptayan BD MGITTM TBc tanımlama kiti (Becton Dickinson, ABD) kullanıldı. BD MGITTM TBc test sonucu pozitif çıkan suşlar M. tuberculosis kompleks (MTC) olarak, test sonucu negatif çıkanlar ise TB dışı mikobakteri (TDM) olarak tanımlandı (16).
Antibiyotik Duyarlılık Testi
M. tuberculosis kompleks suşlarının primer ilaçlara (izoniazid, rifampisin, streptomisin ve etambutol) karşı antibiyotik duyarlılık testleri, BD BACTECTM MGITTM 960 tanımlama sistemi (Becton Dickinson, ABD) kullanılarak yapıldı.
Moleküler Yöntemler
Kalan çözelti, PCR analizi için GeneXpert MTB/RIF (Cepheid, ABD) testi kullanılarak analiz edildi. GeneXpert MTB/RIF testi ile gerçekleştirilen tüm işlemler, üretici firmanın talimatlarına uygun şekilde yapıldı(17). Reaktif (NaOH ve izopropanol karışımı), 1:2 oranında Falcon tüpündeki örneklere eklendi ve karışım, berrak çözelti görülene kadar vortekslendi. Ardından M. tuberculosis’in canlılığını azaltarak biyolojik tehlikeyi en aza indirmek için çözelti, oda sıcaklığında 15 dakika inkübe edildi. Daha sonra steril bir pipet yardımıyla Xpert MTB/RIF kartuşuna 2 ml berrak çözelti ilave edilerek kartuş cihaza yerleştirildi. Sonuçlar iki saat içinde alındı ve örnekler, bakteri yüklerine göre yüksek, orta, düşük ve çok düşük olmak üzere dört seviyede raporlandı (18).
Kültür sonucuna göre tüberküloz dışı mikobakterilerin (TDM) tanımlanmasında GenoType Mycobacterium CM test kiti (Hain Lifescience, Almanya) üretici firma talimatlarına uygun olarak kullanıldı (19). Üç aşamalı bu testte, sıvı veya katı besiyerinde üremiş mikobakteriler kullanılarak yapılan DNA ekstraksiyonu sonrasında biotinlenmiş primerler kullanılarak amplifikasyon sağlandı. Son basamakta ters hibridizasyon ile strip üzerinde oluşan bant paternlerine göre tiplendirme tamamlandı. Birden fazla kültürde aynı türün ürediği hastalara ait izolatlar etken kabul edildi. Tüberküloz dışı mikobakteri sayısı belirlenirken, aynı hastaya ve aynı örnek alım bölgesine ait yineleyen örnekler göz ardı edildi.
Çalışma için Fırat Üniversitesi Girişimsel Olmayan Araştırmalar Etik Kurulu’ndan 03 Ağustos 2023 tarih ve 17482 karar numarasıyla onay alındı.
İstatiksel Analizler
Verilerin analizi, SPSS (Statistical Package for the Social Sciences) versiyon 20.0 programı (IBM Corp., Armonk, NY, ABD) ile yapıldı. Verilerin tanımlanmasında sayı (n) ve yüzde (%) değerleri kullanıldı. GeneXpert MTB/RIF testinin sonuçları, TB tanısında altın standart yöntem olan kültür sonuçlarıyla karşılaştırıldı. Yöntemlerin duyarlılığı, özgüllüğü, negatif öngörü değeri (NÖD) ve pozitif öngörü değeri (PÖD) hesaplanarak performans değerlendirmeleri yapıldı. Normal dağılım gösteren grupların verileri, ortalama ± standart sapma (SS) ile ifade edildi. Normal dağılıma uymayan grupların verileri ise medyan (25. yüzdelik-75. yüzdelik) olarak belirtildi. Normal dağılıma uyan grupların niceliksel verilerinin karşılaştırılmasında Student t testi kullanıldı. Normal dağılıma uymayan iki grubun niceliksel verilerinin karşılaştırılmasında ise Mann-Whitney U testi kullanıldı.
BULGULAR
Çalışmamız kapsamında, ADB aranması ve mikobakteri kültürü yapılması amacıyla 171 pulmoner ve 208 ekstrapulmoner olmak üzere toplam 379 klinik örnek değerlendirildi. Hastaların 20’sinde Mycobacterium tuberculosis kompleks (MTBK) üremesi, üçünde ise TDM üremesi gözlendi. TDM üremesi olan hastaların tekrarlanan kültürlerinde bir hastada üreme olmadı ve negatif olarak değerlendirildi.
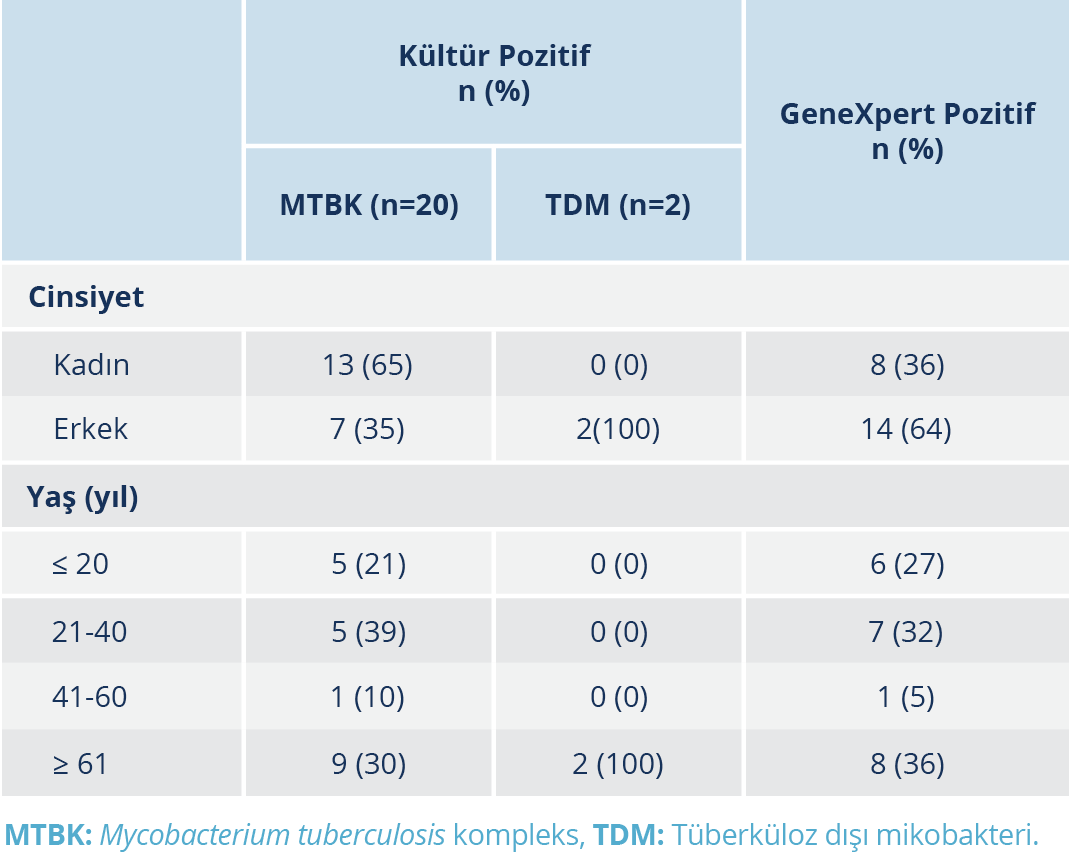
Mycobacterium tuberculosis kompleks üremesi olan örneklerin dağılımı; 15 (%88.52) pulmoner (10 balgam ve 5 bronşiyal lavaj örneği) ve 5 (%11.48) ekstrapulmoner (5 plevral mayi örneği) şeklindeydi. Tüberküloz dışı mikobakteri üremesi olan örneklerin tamamı (%100) balgam örneğiydi. Mycobacterium tuberculosis kompleks üremesi olan hastaların yaş ortalaması ± standart sapma (SS) değeri 48.15 ± 27.75 yıl, TDM üremesi olan hastalarda ise bu değer 77 ± 1.73 yıl olarak bulundu. GeneXpert PCR test sonucu pozitif olan hastalarda yaş için ortalama ± SS değeri 42.26 ± 26.16 yıl idi. Hastalarda MTBK ve TDM üremesi açısından yaş için ortalama ± SS değerlerinde anlamlı düzeyde fark tespit edildi (p ≤ 0.05). Tüberküloz kültür ve PCR test sonucu pozitif olan hastaların yaş ve cinsiyet dağılımları Tablo 1’de gösterildi.
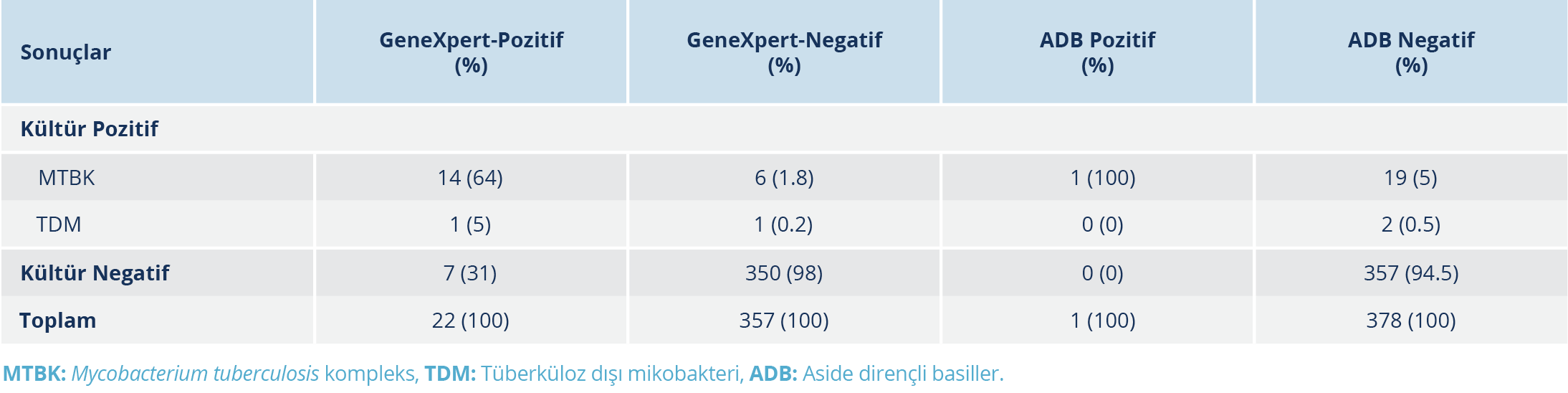
Mycobacterium tuberculosis kompleks üremesi olan 20 örneğin 1 (%1)’inde ADB yayması pozitif olarak tespit edildi. Kültürde üreme sonrası TDM olarak tanımlanan üç örneğin hiçbirinde ADB yayması pozitif bulunmazken, ADB yayması pozitif olan örneğin balgam olduğu belirlendi. Ekstrapulmoner örneklerin tümünde ADB yayması negatif olarak tespit edildi (Tablo 2).
Toplam 379 örnek üzerinde moleküler yöntemlerle (gerçek zamanlı PCR) mikobakteri varlığı araştırıldı. Bu örneklerin 22’sinde test sonucu pozitif (beşi düşük pozitif) ve 357’sinde negatif bulundu. Pozitif sonuçlanan 22 örneğin 14’ü pulmoner, sekizi ekstrapulmoner örneklerden oluşuyordu. PCR testinin pulmoner örneklerdeki performansı daha yüksek bulundu. Test sonucu pozitif olan 22 hastadan 15 (%68)’inde kültürde üreme görüldü. Bu hastaların 14’ünde etken MTBK, birinde ise TDM olarak tanımlandı. Kültürde üreme olmayıp negatif değerlendirilen yedi örneğin (ikisi düşük pozitif) PCR testi sonucu pozitif olarak tespit edildi. Bu örneklerin beşi balgam, biri plevral mayi ve biri beyin omurilik sıvısı (BOS) idi. Pozitif tespit edilen BOS örneği, yeni numune ile tekrar çalışıldığında negatif olarak bulundu. Toplam 379 örneğin sadece birinde ADB yayması pozitif olarak tespit edildi. Bu örnek, PCR testi sonucuna göre de pozitif olup kültürde etken MTBK olarak tanımlandı.
BD BACTECTM MGITTM 960 tanımlama sistemi sonuçları referans kabul edilerek yapılan istatistiksel analizler sonucunda, Xpert MTB/RIF testinin özgüllüğü %98, duyarlılığı %68, pozitif öngörü değeri (PÖD) %68 ve negatif öngörü değeri (NÖD)%98 olarak hesaplandı (Tablo 2). PCR test sonucu pozitif olan örneklerin birinde RİF direnci tespit edildi. Bu hasta örneğinin kültüründe de etken MTBK olarak doğrulandı. BD BACTECTM MGITTM 960 sistemiyle yapılan doğrulama çalışmasında da RİF direnci pozitif bulundu.
İRDELEME
Tüberküloz, özellikle düşük gelirli toplumlarda artan ölüm oranlarıyla ciddi bir halk sağlığı sorunu olarak karşımıza çıkmaktadır. Erken teşhis ve uygun tedaviye başlamak, ölüm oranlarını azaltabilmek için kritik öneme sahiptir. Ekstrapulmoner TB tanısı ciddi bir sorundur ve güncel testlerin doğruluğu ile sınırlıdır (5).
Tüberkülozun teşhisinde, ADB yayma mikroskobisi ve kültürü son derece önemlidir. Kültür, altın standart yöntem olarak kabul edilmesine rağmen zaman alıcıdır; uygun altyapı ve yetkinlik gerektirir (20). Diğer yandan, ADB yayması hızlı ve ucuzdur; ancak duyarlılığı değişkendir (%20-80) ve sınırlı özgüllüğü nedeniyle MTB ile TDM’leri ayırt edemez (3). Söz konusu kısıtlılıklardan dolayı DSÖ tarafından tam otomatik Xpert MTB/RIF testi PTB tanısı için en hızlı test olarak onaylanmıştır (21). GeneXpert MTB/RIF testi, MTB ve RIF direnciyle ilişkili mutasyonları eş zamanlı olarak saptamak için DNA PCR teknolojisini kullanır (22).
Çalışmamızda MTBK üremesi olan örneklerin PCR pozitiflik oranı daha yüksek olarak bulundu; 20 MTBK üremesi olan örneğin 14 (%70)’ünde test sonucu pozitif idi. Kültürde TDM üremesi olan üç örnekten birinin (%33) PCR test sonucu pozitifti. Albay ve arkadaşlarının (23) yaptığı çalışmada, PCR testi PTB için ekstrapulmoner TB’den daha iyi performans göstermiştir (23). Bizim çalışmamızda da literatürü destekler şekilde 171 pulmoner örneğin 12 (%7)’si ve 208 ekstrapulmoner örnekten 3 (%1)’ü PCR pozitif olarak bulundu ve PCR testi PTB için daha iyi performans gösterdi.
Çalışmamızda TB şüphesi olan hastaların pulmoner ve ekstrapulmoner örnekleri değerlendirildi. Değerlendirilen 379 örneğin pozitiflik oranı doğrudan ADB yayma incelemesi ile %0.3, BD BACTECTM MGITTM 960 sistemi ile %6 olarak bulundu. GeneXpert MTB/RIF pozitiflik oranı ise %6 idi. Yapılan çalışmalarla elde edilen oranların daha düşük çıkmasının, örnek sayısının fazla olması ve tüberküloz için yüksek klinik şüphesi olmayan hastalardan da örnek alınmasından kaynaklandığını düşünüyoruz. Yaptığımız çalışmada GeneXpert MTB/RIF testinin duyarlılığı ve özgüllüğü sırasıyla %68 ve %98 idi. Duyarlılık bulgumuz, farklı ülkelerde yapılan çalışmalardan (%82.1-%90.3) daha düşük bulundu (24-27). Bunun nedeni, örnek taşıma ve saklama koşullarının uyumsuzluğundan olabilir. Özgüllük bulgumuz ise daha önce yapılan bazı çalışmaları (%93.8-%100) destekler niteliktedir (24,25,27-29).
Yapılan başka bir çalışmada, GeneXpert MTB/RIF testinin duyarlılığı %95, özgüllüğü %99, PÖD %93 ve NÖD %99 olarak bildirilmiştir. Pulmoner ve ekstrapulmoner örnekler için duyarlılık, özgüllük, PÖD ve NÖD sırasıyla %100 ve %83.3; %99.3 ve %99.5; %94.1 ve %85.7; %100 ve %99.5 olarak belirlenmiştir (23). Böylesi farklılıkların örnek kalitesi, toplanma süreci ve taşınma koşullarından kaynaklanabileceği bildirilmiştir (30).
Çavuşoğlu ve arkadaşlarının (31) ülkemizde yaptığı çalışma kapsamında tüm solunum örnekleri için GeneXpert testinin sonuçları duyarlılık %93.8, özgüllük %98.8, PÖD %86.5 ve NÖD %99.5 şeklindedir. Diğer yanda, ADB yayma sonucu pozitif olan 30 örnekte duyarlılık %100 iken yayması negatif olan 18 örnekte bu oran %83 3 olarak bildirilmiştir. Tüm solunum dışı örnekler içinse duyarlılık, özgüllük, PÖD ve NÖD değerleri sırasıyla %71.9, %99.3, %85 2 ve %98 5 olarak tespit edilmiştir. Yayma sonucu pozitif olan 12 örnekte duyarlılık %100 olup yayma sonucu negatif olan 20 örnekte bu oran %55’e düşmüştür. GeneXpert MTB/RIF testinin, özellikle yayma sonucu pozitif olan klinik örnekler ile yayma sonucu negatif olan solunum örneklerinde RİF dirençli M. tuberculosis’in saptanmasında yararlı olduğu bulunmuştur (31).
Çalışmamızda kültürde üreme olmayıp negatif olarak değerlendirilen yedi örnek (iki örnek düşük pozitif idi) GeneXpert MTB/RIF testi ile pozitif olarak tespit edildi; örneklerin dağılımı beş balgam örneği, bir plevral mayi örneği ve bir BOS örneği şeklindeydi. Pozitif olarak tespit edilen BOS örneği yeni numune ile tekrar çalışıldı ve sonuç negatif olarak bulundu. Bir çalışmada, Xpert MTB/RIF testi sonuçlarının yanlış pozitifliği bildirilmiş olup bu sonuç özellikle daha önce tedavi görmüş hastalarda test numunelerinde ölü MTB bulunmasına bağlanmıştır (32). Moleküler yöntemlerde kontaminasyon dikkate alınması gereken bir husustur. Ayrıca tedavi gören hastalardan canlı bakteri örneği alınamayabilir. PCR yöntemlerinde canlı ve ölü basillerin ayrımı yapılamadığı için MTB öyküsü olan hastalarda yalancı pozitiflik görülebildiği bildirilmiştir (33). Çalışmamızda kültürde üreme olmayıp PCR test sonucu pozitif olan hastaların kayıtlarına ulaşılamadığı için daha önce anti-TB ilaçlarla tedavi edilip edilmediklerine dair bilgi alınamadı. Anti-TB ilaçlar konusunda önceki tedaviye özel vurgu yapmak ve dikkatli bir şekilde öykü almak, yanlış pozitif sonuçların önlenmesinde kritik öneme sahiptir. Kültür, klinik örneklerde MTB›nin saptanması için en duyarlı yöntem olmaya devam etmektedir ve tüberküloz basilinin izolasyonunda altın standarttır. Haziran 2012 itibarıyla, TB yükünün yüksek olduğu ülkelerin üçte ikisinde ve çoklu ilaç dirençli TB yükünün yüksek olduğu ülkelerin yarısında, GeneXpert MTB/RIF testi ulusal tüberküloz programlarına ve kılavuzlarına dahil edilmiştir (34).
Erken teşhis, hastalığın bulaşmasının kontrol altına alınmasını ve TB tedavisinin zamanında başlamasını kolaylaştırır. Çalışmamızda yayma negatif örneklerde GeneXpert MTB/RIF testinin pozitif saptama oranı %28 olarak tespit edildi. Yapılan çalışmalarda, GeneXpert MTB/RIF’in yayma negatif akciğer TB örneklerini tespit etmede yaklaşık %28-41 oranında pozitiflik gösterdiği bildirilmiş olup bu sonuçlar çalışmamızla uyumludur (35,36).
Ekstrapulmoner örneklerde yayma negatifliği daha sık görülmektedir. Çalışmamızda, ADB yayma pozitif örneği balgam örneği idi. Ekstrapulmoner örneklerde ADB yayma pozitifliği ise görülmedi. PCR pozitif örneklerimizin 15’i pulmoner ve yedisi ekstrapulmoner örneklere aitti. Ekstrapulmoner örneklerde ADB yayma negatifliği daha yaygın görüldüğü için TB’nin erken tanısı için PCR testinin daha uygun olduğunu düşünüyoruz.
Çalışmamızda yedi örneğin kültüründe üreme görülürken, PCR test sonucu negatif olarak bulundu ve yalancı negatiflik oranı %32 idi; bu sonuç literatüre göre daha yüksek bir orandı. Bunun nedeninin örneklerin basil yükünün az olması olduğunu düşünüyoruz. On beş farklı çalışmanın dahil edilerek yapıldığı bir meta-analizde, yalancı negatiflik oranı %9.6 olarak bildirilmiş olup bu durumun nedeninin örneklerin içindeki basil yükünün analitik saptama limiti olan 131 CFU/ml’nin altında olmasından kaynaklandığı ifade edilmiştir (37).
Çalışmamızın en önemli kısıtlılıkları; yalancı pozitiflik oranlarımızın yüksek olması, kültürde üreme olmayıp PCR test sonucu pozitif olan hastaların kayıtlarına ulaşılamaması ve bu hastaların daha önce anti-TB ilaçlarla tedavi edilip edilmediğine dair bilgi alınamamasıdır. Bu nedenle yüksek yalancı pozitiflik oranını açıklayacak nedenleri bulamadık. Daha yüksek örnek sayısıyla ve benzer klinik şüphelere sahip hastalar üzerinde yöntemlerin karşılaştırılmasını yapacak, anti-TB ilaçlarla daha önceki tedavilere özel vurgu yapılmış ve dikkatli öykü alımına dayanan çalışmalara ihtiyaç duyulmaktadır.
Sonuç olarak çalışmamızda; GeneXpert testi, pulmoner ve ekstrapulmoner örneklerde MTB’nin saptanması için ADB yayma mikroskobuna göre daha yüksek bir duyarlılık gösterdi. Kültür, MTB için altın standart olarak kabul edilmekle birlikte, MTB kolonilerinin büyümesi daha uzun zaman almakta ve RİF direncini eş zamanlı olarak tespit edememektedir. Bununla birlikte, GeneXpert testi, çoklu ilaç dirençli TB tespitini aynı anda gerçekleştirebilmesi sayesinde, yayma negatif TB şüphelilerinin yanı sıra ADB yayma pozitif olgularda MTB’nin hızlı tespiti için değerli bir teşhis aracı olarak kabul edilmektedir. Erken tespit, hastalığın bulaşmasının kontrol altına alınmasını ve TB tedavisinin zamanında başlamasını kolaylaştırır. Bu doğrultuda, GeneXpert testinin uygulanması, çoklu ilaç dirençli TB olgularının önemli ölçüde azalmasını sağlayacaktır.
Hasta Onamı
Veriler retrospektif olarak değerlendirildiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma için Fırat Üniversitesi Girişimsel Olmayan Araştırmalar Etik Kurulu’ndan 03 Ağustos 2023 tarih ve 17482 karar numarasıyla onay alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman.
Yazar Katkıları
Fikir/Kavram – F.G., Z.A.T.; Tasarım – F.G.; Denetleme – F.G., Z.A.T.; Kaynak ve Fon Sağlama – Z.A.T.; Malzemeler/Hastalar – F.G.; Veri Toplama ve/veya İşleme – F.G.; Analiz ve/veya Yorum – F.G.; Literatür Taraması – F.G.; Makale Yazımı – F.G.; Eleştirel İnceleme – F.G.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Referanslar
- Xie C, Hu X, Liu Y, Shu C. Performance comparison of GeneXpert MTB/RIF, gene chip technology, and modified Roche culture method in detecting Mycobacterium tuberculosis and drug susceptibility in sputum. Contrast Media Mol Imaging. 2022;2022:2995464. [CrossRef]
- Tuberculosis: Key facts [Internet]. Geneva: World Health Organization (WHO). [erişim 13 Kasım 2024]. https://www.who.int/news-room/fact-sheets/detail/tuberculosis
- Global tuberculosis report 2023 [Internet]. Geneva: World Health Organization (WHO). [erişim 13 Kasım 2024]. https://www.who.int/publications/i/item/9789240083851
- Türkiye’de Verem Savaşı 2021 Raporu [Internet]. Ankara: T.C. Sağlık Bakanlığı Halk Sağlığı Genel Müdürlüğü. [erişim 13 Kasım 2024]. https://hsgm.saglik.gov.tr/depo/birimler/tuberkuloz-db/Dokumanlar/Raporlar/Turkiyede_Verem_Savasi_2021_Raporu.pdf
- Global tuberculosis report 2020 [Internet]. Geneva: World Health Organization (WHO). [erişim 13 Kasım 2024]. https://www.who.int/publications/i/item/9789240013131
- Türkiye’de Verem Savaşı 2020 Raporu [Internet]. Ankara: T.C. Sağlık Bakanlığı Halk Sağlığı Genel Müdürlüğü. [erişim 13 Kasım 2024]. https://hsgm.saglik.gov.tr/depo/birimler/tuberkuloz-db/Dokumanlar/Raporlar/Turkiyede_Verem_Savasi_2020_Raporu.pdf
- Mechal Y, Benaissa E, El Mrimar N, et al. Evaluation of GeneXpert MTB/RIF system performances in the diagnosis of extrapulmonary tuberculosis. BMC Infect Dis. 2019;19(1):1069. [CrossRef]
- Rimal R, Shrestha D, Pyakurel S, et al. Diagnostic performance of GeneXpert MTB/RIF in detecting MTB in smear-negative presumptive TB patients. BMC Infect Dis. 2022;22(1):321. [CrossRef]
- Steingart KR, Henry M, Ng V, et al. Fluorescence versus conventional sputum smear microscopy for tuberculosis: a systematic review. Lancet Infect Dis. 2006;6(9):570-81. Erratum in: Lancet Infect Dis. 2006;6(10):628. [CrossRef]
- Stevens WS, Scott L, Noble L, Gous N, Dheda K. Impact of the GeneXpert MTB/RIF technology on tuberculosis control. Microbiol Spectr. 2017;5(1). [CrossRef]
- Policy Statement: Automated Real-Time Nucleic Acid Amplification Technology for Rapid and Simultaneous Detection of Tuberculosis and Rifampicin Resistance: Xpert MTB/RIF System [Internet]. Geneva: World Health Organization (WHO); 2011. [erişim 13 Kasım 2024]. https://www.ncbi.nlm.nih.gov/books/NBK304235/
- Tuberculosis: Diagnostics, Automated DNA Test [Internet]. Geneva: World Health Organization (WHO); 2010. [erişim 13 Kasım 2024]. https://stoptb.org/wg/gli/assets/documents/xpert_factsheet.pdf
- Siracuse CG, Bernardo J. Sloutsky A. Genexpert MTB/RIF Performance evaluation in respiratory specimens in Ecuador. Am J Respir Crit Care Med. 2015;191:A3308.
- Stagg HR, White PJ, Riekstiņa V, et al. Decreased time to treatment ınitiation for multidrug-resistant tuberculosis patients after use of Xpert MTB/RIF test, Latvia. Emerg Infect Dis. 2016;22(3):482-90. [CrossRef]
- Pongpeeradech N, Kasetchareo Y, Chuchottaworn C, Lawpoolsri S, Silachamroon U, Kaewkungwal J. Evaluation of the use of GeneXpert MTB/RIF in a zone with high burden of tuberculosis in Thailand. PLoS One. 2022;17(7):e0271130. [CrossRef]
- Tüberküloz Tanı ve Tedavi Rehberi, 2019 [Internet]. Ankara: T.C. Sağlık Bakanlığı. [erişim 13 Kasım 2024]. https://hsgm.saglik.gov.tr/depo/birimler/tuberkuloz-db/Dokumanlar/Rehberler/Tuberkuloz_Tani_ve_Tedavi_Rehberi.pdf
- Cepheid: Xpert MTB/RIF. [Package insert]. Sunnyvale, CA: Cepheid; 2013.
- Pang Y, Wang Y, Zhao S, Liu J, Zhao Y, Li H. Evaluation of the Xpert MTB/RIF assay in gastric lavage aspirates for diagnosis of smear-negative childhood pulmonary tuberculosis. Pediatr Infect Dis J. 2014;33(10):1047-51. [CrossRef]
- Meerhoff TJ, Simaku A, Ulqinaku D, et al. Surveillance for severe acute respiratory infections (SARI) in hospitals in the WHO European region – an exploratory analysis of risk factors for a severe outcome in influenza-positive SARI cases. BMC Infect Dis. 2015;15:1. [CrossRef]
- Dunn JJ, Starke JR, Revell PA. Laboratory diagnosis of Mycobacterium tuberculosis infection and disease in children. J Clin Microbiol. 2016;54(6):1434-41. [CrossRef]
- Xpert MTB/RIF implementation manual: technical and operational ‘how-to’; practical considerations [Internet]. Geneva: World Health Organization (WHO); 2014. [erişim 13 Kasım 2024]. https://iris.who.int/handle/10665/112469
- Fouda ME, Abdel Gwad ER, Fayed SM, Kamel MH, Ahmed SA. A study of the added value of Xpert MTB/RIF assay for assessment of pulmonary tuberculosis transmission risk. Egypt J Med Microbiol. 2019;28(3):141-8. [CrossRef]
- Albay A, Güney M, Tekin K, Kısa Ö, Sığ AK. [Evaluation of the geneXpert MTB/RIF assay for early diagnosis of tuberculosis and detection of rifampicin resistance in pulmonary and extrapulmonary specimens]. Cukurova Med J. 2016;41(3):548-53. Turkish. [CrossRef]
- Zeka AN, Tasbakan S, Cavusoglu C. Evaluation of the GeneXpert MTB/RIF assay for rapid diagnosis of tuberculosis and detection of rifampin resistance in pulmonary and extrapulmonary specimens. J Clin Microbiol. 2011;49(12):4138-41. [CrossRef]
- Boehme CC, Nicol MP, Nabeta P, et al. Feasibility, diagnostic accuracy, and effectiveness of decentralised use of the Xpert MTB/RIF test for diagnosis of tuberculosis and multidrug resistance: a multicentre implementation study. Lancet. 2011;377(9776):1495-505. [CrossRef]
- Bojang AL, Mendy FS, Tientcheu LD, et al. Comparison of TB-LAMP, GeneXpert MTB/RIF and culture for diagnosis of pulmonary tuberculosis in the Gambia. J Infect. 2016;72(3):332-7. [CrossRef]
- Heidebrecht CL, Podewils LJ, Pym AS, Cohen T, Mthiyane T, Wilson D. Assessing the utility of Xpert( ) MTB/RIF as a screening tool for patients admitted to medical wards in South Africa. Sci Rep. 2016;6:19391. [CrossRef]
- Bajrami R, Mulliqi G, Kurti A, Lila G, Raka L. Comparison of GeneXpert MTB/RIF and conventional methods for the diagnosis of tuberculosis in Kosovo. J Infect Dev Ctries. 2016;10(4):418-22. [CrossRef]
- Bunsow E, Ruiz-Serrano MJ, López Roa P, Kestler M, Viedma DG, Bouza E. Evaluation of GeneXpert MTB/RIF for the detection of Mycobacterium tuberculosis and resistance to rifampin in clinical specimens. J Infect. 2014;68(4):338-43. [CrossRef]
- Tang T, Liu F, Lu X, Huang Q. Evaluation of GeneXpert MTB/RIF for detecting Mycobacterium tuberculosis in a hospital in China. J Int Med Res. 2017;45(2):816-22. [CrossRef]
- Çavuşoğlu C, Soylu M. [Evaluation of GeneXpert MTB/RIF assay for the diagnosis of tuberculosis and rapid detection of rifampicin resistance in clinical specimens]. Türk Mikrobiyol Cem Derg. 2014;44(2):61-4. Turkish. [CrossRef]
- Boyles TH, Hughes J, Cox V, Burton R, Meintjes G, Mendelson M. False-positive Xpert® MTB/RIF assays in previously treated patients: need for caution in interpreting results. Int J Tuberc Lung Dis. 2014;18(7):876-8. [CrossRef]
- Afsar I, Gunes M, Er H, Gamze Sener A. Comparison of culture, microscopic smear and molecular methods in diagnosis of tuberculosis. Rev Esp Quimioter. 2018;31(5):435-8.
- Molicotti P, Bua A, Zanetti S. Cost-effectiveness in the diagnosis of tuberculosis: choices in developing countries. J Infect Dev Ctries. 2014;8(1):24-38. [CrossRef]
- Sah SK, Bhattarai PR, Shrestha A, Dhami D, Guruwacharya D, Shrestha R. Rifampicin-resistant Mycobacterium tuberculosis by GeneXpert MTB/RIF and associated factors among presumptive pulmonary tuberculosis patients in Nepal. Infect Drug Resist. 2020;13:2911-9. [CrossRef]
- Menon LJB, Feliciano CS, de Campos MR, Bollela VR. Decision making to discharge patients from airborne infection isolation rooms: The role of a single GeneXpert MTB/RIF strategy in Brazil. Infect Control Hosp Epidemiol. 2020;41(7):784-8. [CrossRef]
- Chang K, Lu W, Wang J, et al. Rapid and effective diagnosis of tuberculosis and rifampicin resistance with Xpert MTB/RIF assay: a meta-analysis. J Infect. 2012;64(6):580-8. [CrossRef]