En Çok Okunanlar
Özet
Amaç: Üçüncü kuşak sefalosporin dirençli Enterobacterales (3KSDE) takımından bakteriler ile gelişen bakteriyemi sıklıkla karşımıza çıkmaktadır. Bu çalışmada, 3KSDE bakteriyemisi olan olgularda ampirik antibiyotik tedavisinin uygunluğunun sonuçlar ile ilişkisi ve 30 günlük mortalite ilişkili faktörlerin araştırılması amaçlandı.
Yöntemler: Kan kültürlerinde Enterobacterales takımı bakteri üreyen ve üçüncü kuşak sefalosporin direnci gösteren erişkin hastaların demografik ve klinik verileri retrospektif olarak incelendi. Hastalar ampirik antibiyotik tedavisine uygun olanlar ve olmayanlar olarak iki gruba ayrıldı. İki grup arasında demografik veriler, klinik karakteristikler ve sonuçlar karşılaştırıldı. Sonuçlar, toplum kökenli infeksiyonlar, hastane kökenli infeksiyonlar ve üriner sistem infeksiyonları alt gruplarında da analiz edildi. Ayrıca, tüm popülasyonda 30 günlük mortalite gelişen hastalarda mortalite ilişkili faktörler lojistik regresyon analiziyle değerlendirildi.
Bulgular: Çalışmaya 144 erişkin hasta dahil edildi. Uygun ampirik antibiyotik tedavi alan hasta sayısı 90 (%62.5) idi. En sık karşılaşılan bakteriyemi nedenleri, üriner sistem infeksiyonu (%32.6) ve santral kateter ilişkili infeksiyondu (%21.5). Escherichia coli (98 hasta) ve Klebsiella türleri (31 hasta) en sık karşılaşılan etkenlerdi. Ampirik antibiyotik tedavisinin uygunluğu ile hastane yatışı, hastane içi mortalite, 14, 30 ve 90 günlük mortalite arasında anlamlı düzeyde ilişki hem tüm popülasyonda hem de bahsedilen alt gruplarda saptanmadı. Tedavinin uygunluğu ile 30 günlük mortalite arasındaki ilişkiyi değerlendiren Kaplan-Meier sağkalım analizinde, gruplar arasında anlamlı düzeyde fark saptanmadı. Tüm nedenlere bağlı 30 günlük mortalite 31 (%21.5) hastada gelişti. Demans ve vazopressör tedavi ihtiyacı, 30 günlük mortalite için bağımsız risk faktörleri olup etkene yönelik uygun antibiyotik tedavisine 48 saatten önce başlanması mortaliteden koruyucu faktör olarak belirlendi.
Sonuç: Çalışmamızda 3KSDE bakteriyemisinde ampirik antibiyotik tedavisinin uygun olup olmaması ile sonuçlar açısından anlamlı düzeyde bir ilişki saptanmadı. Ancak, uygun antibiyotik tedavisine 48 saatten önce başlanması mortaliteden koruyucu bir faktör olarak belirlendi. Uygun antibiyotik tedavisinin başlatılması gecikse dahi hedefe yönelik tedaviye hızlı bir şekilde başlanması sağkalım için son derece önemlidir.
GİRİŞ
Gram-negatif bakterilerin neden olduğu bakteriyemi hem toplum kökenli hem de hastane kökenli infeksiyonlar arasında önemli yer tutmaktadır. Enterobacterales takımından bakterilerle gelişen infeksiyonlar daha önceki çalışmalarda Gram-negatif bakteriyeminin sık sebepleri arasında bildirilmiştir (1,2). Son yıllarda hem üçüncü kuşak sefalosporin dirençli Enterobacterales (3KSDE) infeksiyonlarında hem de bu dirençli bakterilerin toplumdaki yaygınlığında artış olduğu gözlenmiştir (3-6). Bu direnç, genel olarak genişlemiş spektrumlu beta-laktamaz (GSBL) veya AmpC beta-laktamaz enzimleri aracılığıyla oluşmaktadır (7,8). Sepsis ve septik şok gibi hayatı tehdit eden klinik tablolara yol açabilmesi sebebiyle 3KSDE infeksiyonları önemli bir sağlık sorunu olarak değerlendirilmektedir.
Antimikrobiyal direnç, Enterobacterales bakteriyemisi tedavisinde, tedavi seçeneklerini kısıtlayarak önemli bir sorun oluşturmaktadır. Karbapenemler, üriner sistem infeksiyonları dışında, 3KSDE infeksiyonlarının tedavisi için tek seçenek olarak kabul edilmektedir (9). Ancak, Gram-negatif bakterilerin etken olduğu bakteriyemide uygun ampirik antibiyotik tedavisinin klinik sonuçlara etkisini araştıran çalışmalarda farklı sonuçlar bildirilmiştir (10-13). Bu farklılıkların, hasta popülasyonlarının seçimindeki kriterler ve uygun antibiyotik tedavisinin tanımlanmasındaki değişikliklerden kaynaklanabileceği düşünülmektedir.
Çalışmamızda, 3KSDE bakteriyemisi için ampirik antibiyotik tedavisinin uygunluğunun hastane yatış süresi ve mortalite sonuçları ile ilişkisini değerlendirmek amaçlandı. Ayrıca, toplum kökenli infeksiyonlar, hastane kökenli infeksiyonlar, üriner sistem infeksiyonu odaklı bakteriyemi gibi alt gruplarda sonuçlar değerlendirildi ve mortalite gelişen hastalarda 30 günlük mortalite ile ilişkili faktörler belirlendi.
YÖNTEMLER
Bu çalışma, Ocak 2022 – Haziran 2024 tarihleri arasında Giresun Eğitim ve Araştırma Hastanesi’nde retrospektif olarak gerçekleştirildi. Çalışmaya, kan kültüründe Enterobacterales takımı bakteri üreyen ve üçüncü kuşak sefalosporin direnci saptanan erişkin (>18 yaş) hastalar dahil edildi; kan kültüründe birden fazla patojen üreyen, üçüncü kuşak sefalosporin direncinin yanı sıra karbapenem direnci de saptanan, kan kültürü alınması sonrasında ilk 24 saat içerisinde hayatını kaybeden ve herhangi bir sebeple verilerine ulaşılamayan hastalar çalışma dışı bırakıldı. Hastaların verileri, hastane elektronik dosya kayıt sisteminden elde edildi. Yaş, cinsiyet, komorbid hastalıklar, Charlson komorbidite indeksi, infeksiyon odağı, infeksiyonun toplum veya hastane kökenli olması, etken bakteri, antibiyotik duyarlılık paterni, başlanan ampirik antibiyotik tedavisinin ne olduğu ve uygunluğu, etkene yönelik antibiyotik tedavisi, Pitt bakteriyemi skoru, kaynak kontrolü gerekliliği, yoğun bakım yatış ihtiyacı, vazopressör tedavi ihtiyacı, entübasyon ihtiyacı, hastane yatış süresi ve mortalite (hastane yatışı sırasında gelişen, 14, 30 ve 90 günlük) tüm hastalar için araştırıldı ve kayıt altına alındı. Çalışma popülasyonu, ampirik başlanan antibiyotik tedavisi uygun olanlar ve olmayanlar şeklinde iki grupta incelendi. Bu iki grup arasında demografik veriler, klinik karakteristikler ve bakteriyemi ile ilişkili sonuçlar karşılaştırıldı. Alt grup olarak, toplum kökenli infeksiyonlar, hastane kökenli infeksiyonlar ve üriner sistem infeksiyonu odaklı bakteriyemi için analizler gerçekleştirildi. Ayrıca, tüm kohortta 30 günlük mortalite gelişen hastalarda mortalite ilişkili faktörler araştırıldı.
Mikrobiyolojik Analizler
Kan kültürleri BacT/Alert 3D sistemi (bioMérieux, Fransa) kullanılarak inkübe edildi. Mikroorganizma tanımlaması ve antibiyotik duyarlılık testleri VITEK® 2 Compact tam otomotize sistemi (bioMérieux, Fransa) ile gerçekleştirildi. Duyarlılık test sonuçları, Avrupa Antimikrobiyal Duyarlılık Testleri Komitesi (EUCAST) önerileri ve sınır değerleri kullanılarak değerlendirildi.
Tanımlar
Üçüncü kuşak sefalosporin dirençli Enterobacterales, en az bir üçüncü kuşak sefalosporine (seftriakson, sefotaksim, seftazidim, vb.) dirençli ancak tüm karbapenemlere duyarlı Enterobacterales bakteriyemisi olarak tanımlandı.
Ampirik antibiyotik tedavisi, kan kültürü alınması sonrası aynı gün içerisinde başlanan antibiyotik tedavisi olarak belirlendi.
Ampirik antibiyotik tedavi uygunluğu, kan kültüründe üreyen bakteriye karşı en az bir, in vitro duyarlı antibiyotik kullanımı olarak tanımlandı.
İmmünosüpresyon varlığı, sistemik kortikosteroid tedavisi alma (pednizon 16 mg/gün veya eşdeğeri, 14 günden fazla kullanımı), kemoterapi alma, organ nakli öyküsü, biyolojik ajan kullanımı, nötropeni (nötrofil sayısı <500/µl) olması durumlarından herhangi birinin olması olarak değerlendirildi.
Bakteriyemi için herhangi bir odak tespit edilemeyen ve bakterinin doğrudan kan dolaşımına girdiği olgular primer bakteriyemi olarak tanımlandı.
Kaynak kontrolü, infeksiyon kaynağının ortadan kaldırılması olarak tanımlandı. Kaynak kontrolü için uygulamalar, apse drenajı, obstrüktif odağa yönelik girişim, santral kateter çekilmesi ve infekte/nekroze dokunun cerrahi debridmanı olarak değerlendirmeye alındı.
Hastane kökenli infeksiyon, hastane başvurusu sonrası en az 48 saat geçtikten sonra kan kültürü alınan ve bakteriyemi saptanan olgular olarak tanımlandı.
Çalışma, Giresun Eğitim ve Araştırma Hastanesi Bilimsel Araştırmalar Etik Kurulu tarafından 18 Eylül 2024 tarih ve 18.09.2024/03 karar numarası onaylanmıştır.
İstatistiksel Analizler
İstatistiksel analizler, IBM SPSS Statistics for Windows sürüm 26.0 (IBM Corp., Armonk, NY, ABD) kullanılarak gerçekleştirildi. Verilerin tanımlayıcı istatistikleri ortalama, standart sapma (SS), minimum değer, maksimum değer ve yüzde (%) oranları ile ifade edildi. Nümerik verilerin normal dağılımı Kolmogorov-Smirnov testi ile değerlendirildi. Nümerik verilerin karşılaştırılmasında, bağımsız örneklem t-testi veya Mann-Whitney U testi kullanıldı. Bağımsız iki grup arasındaki oranların karşılaştırılmasında Pearson χ2 veya Fisher kesin testi kullanıldı. Ampirik antibiyotik tedavisi uygun olan ve olmayan hastalardaki mortaliteye kadar geçen süre, Kaplan-Meier sağkalım analizi ve “log-rank” testi ile karşılaştırıldı. Otuz-günlük mortalite ile ilişkili bağımsız risk faktörlerini belirlemek için tek değişkenli ve çok değişkenli lojistik regresyon analizi (“backward” LR) kullanıldı. İstatistiksel anlamlılık sınırı p<0.05 olarak kabul edildi.
BULGULAR
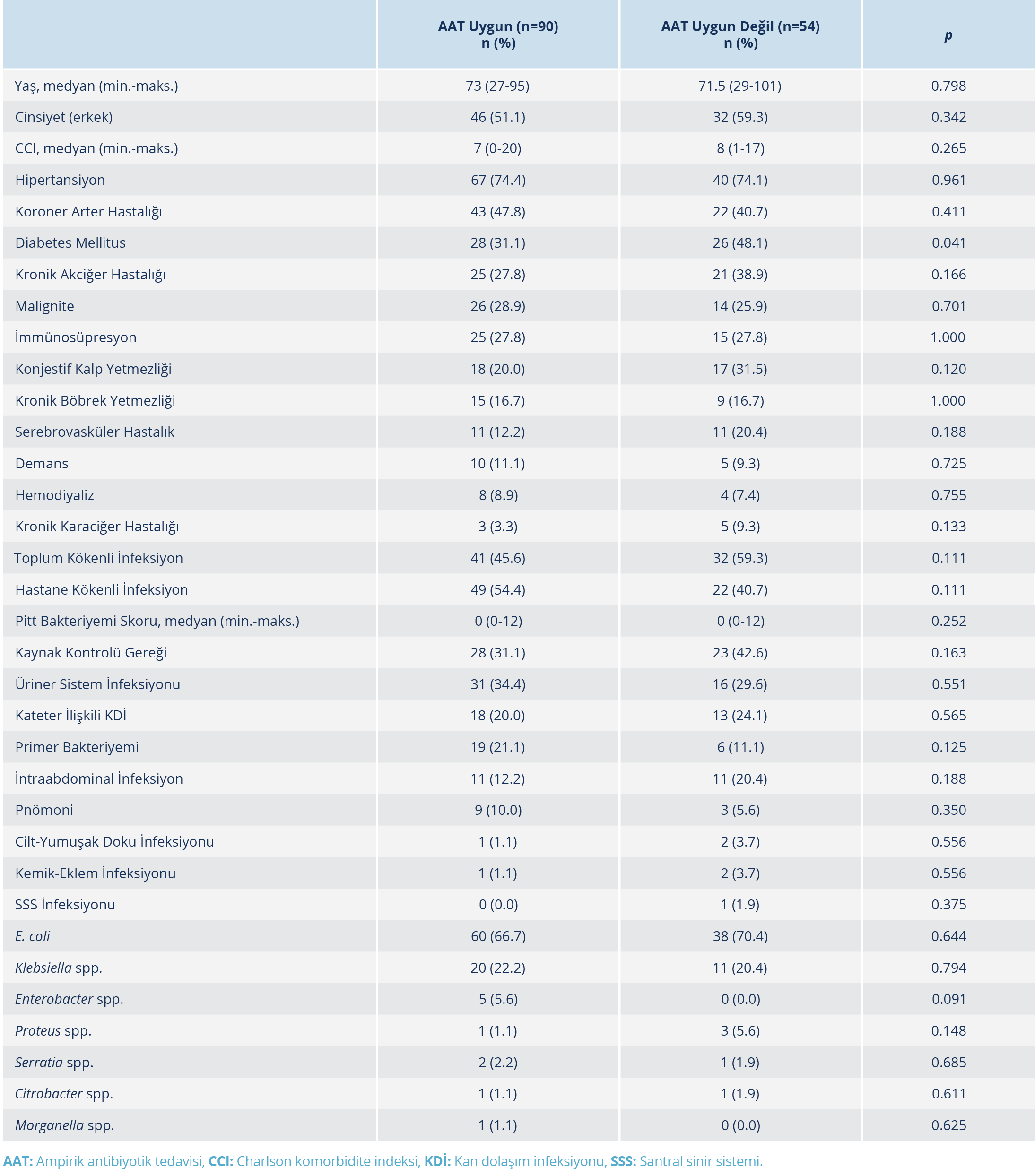
Tablo 1. Üçüncü Kuşak Sefalosporin Dirençli Enterobacterales Bakteriyemilerinin Demografik ve Klinik Özellikleri
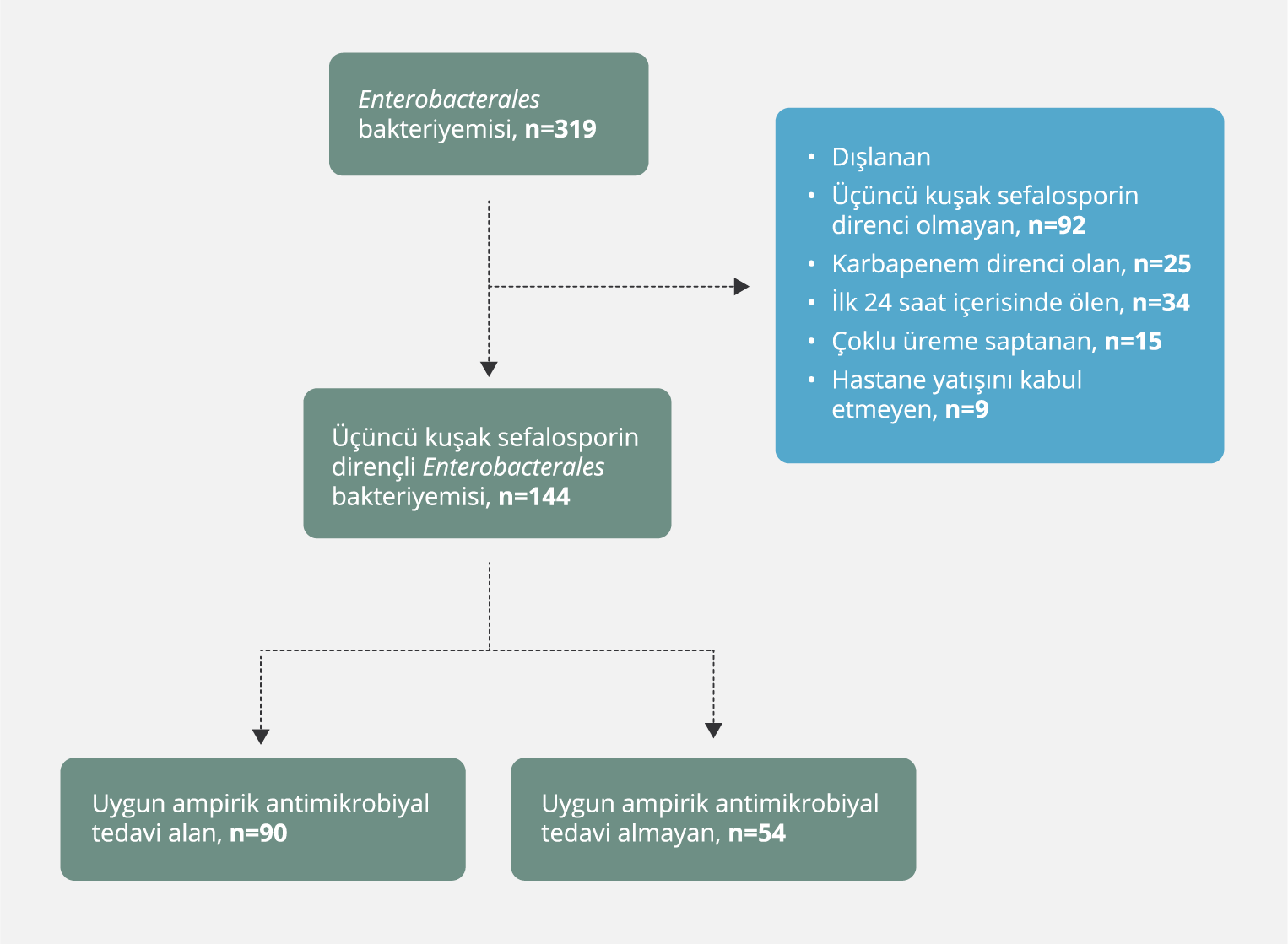
Çalışmanın gerçekleştirildiği dönemde toplam 319 Enterobacterales bakteriyemisi olgusu tespit edildi. Dışlama kriterlerine uyan olgular çıkarıldıktan sonra, 3KSDE bakteriyemisi olan 144 olgu analiz edildi (Şekil 1). Olguların 78 (%54.2)’i erkek olup olguların tamamının yaş ortalaması 70.6±15.9 (27-101) yıl idi. Uygun ampirik antimikrobiyal tedavi alan hasta sayısı 90 (%62.5) olarak belirlendi. En sık rastlanan komorbid hastalıklar sırasıyla hipertansiyon (HT), koroner arter hastalığı (KAH) ve diabetes mellitus (DM) idi. Olguların 71 (%49.3)’i hastane kökenli infeksiyon olarak sınıflandırıldı. Bakteriyeminin odağı incelendiğinde en sık karşılaşılan nedenler; üriner sistem infeksiyonu (%32.6), santral kateter ilişkili infeksiyon (%21.5), primer bakteriyemi (%17.4) ve intraabdominal infeksiyon (%15.3) olarak tespit edildi. Kan kültüründen izole edilen etkenler ise Escherichia coli (n=98) ve Klebsiella spp. (n=31) idi. Çalışmaya dahil edilen olguların demografik ve klinik özellikleri Tablo 1’de sunuldu.
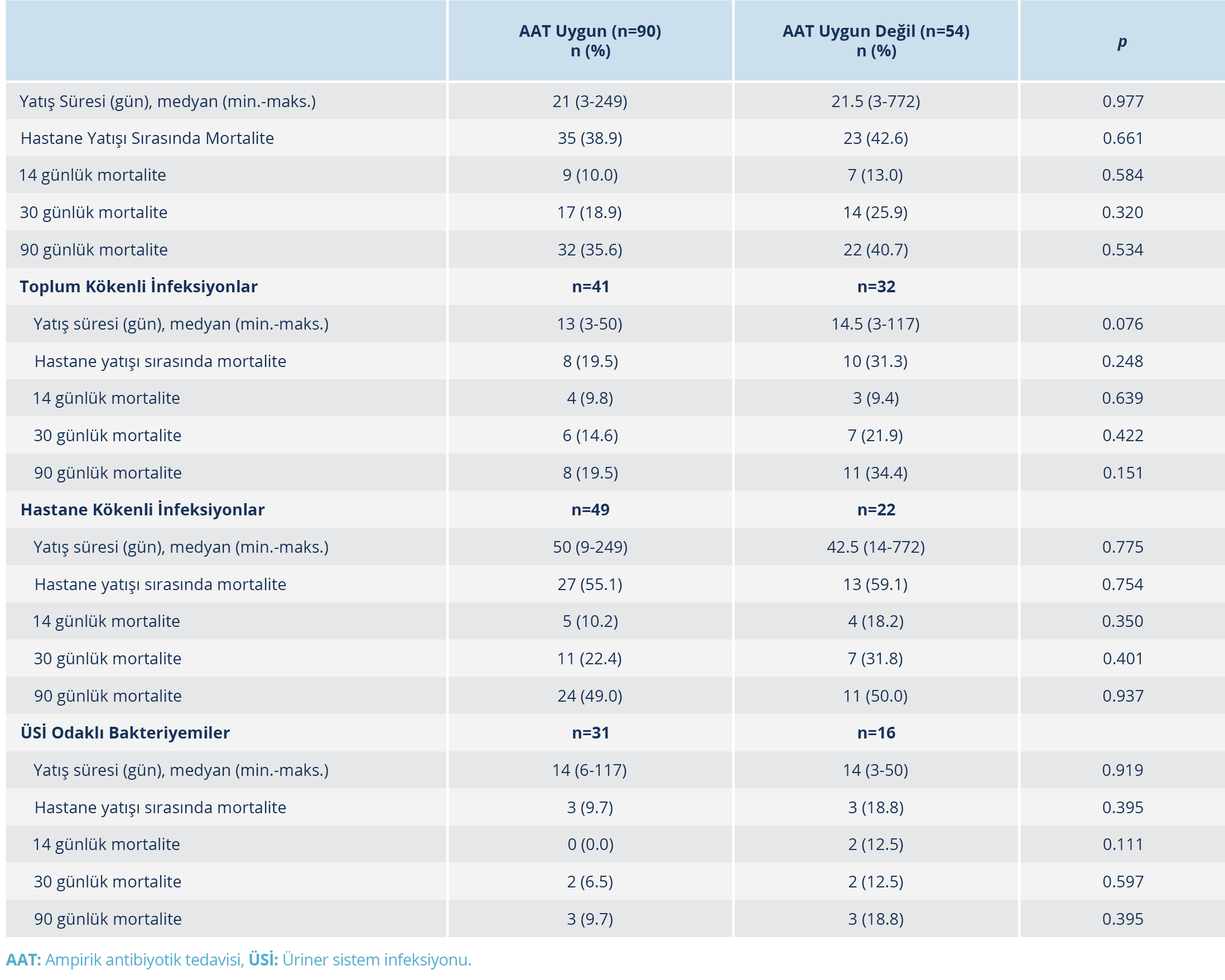
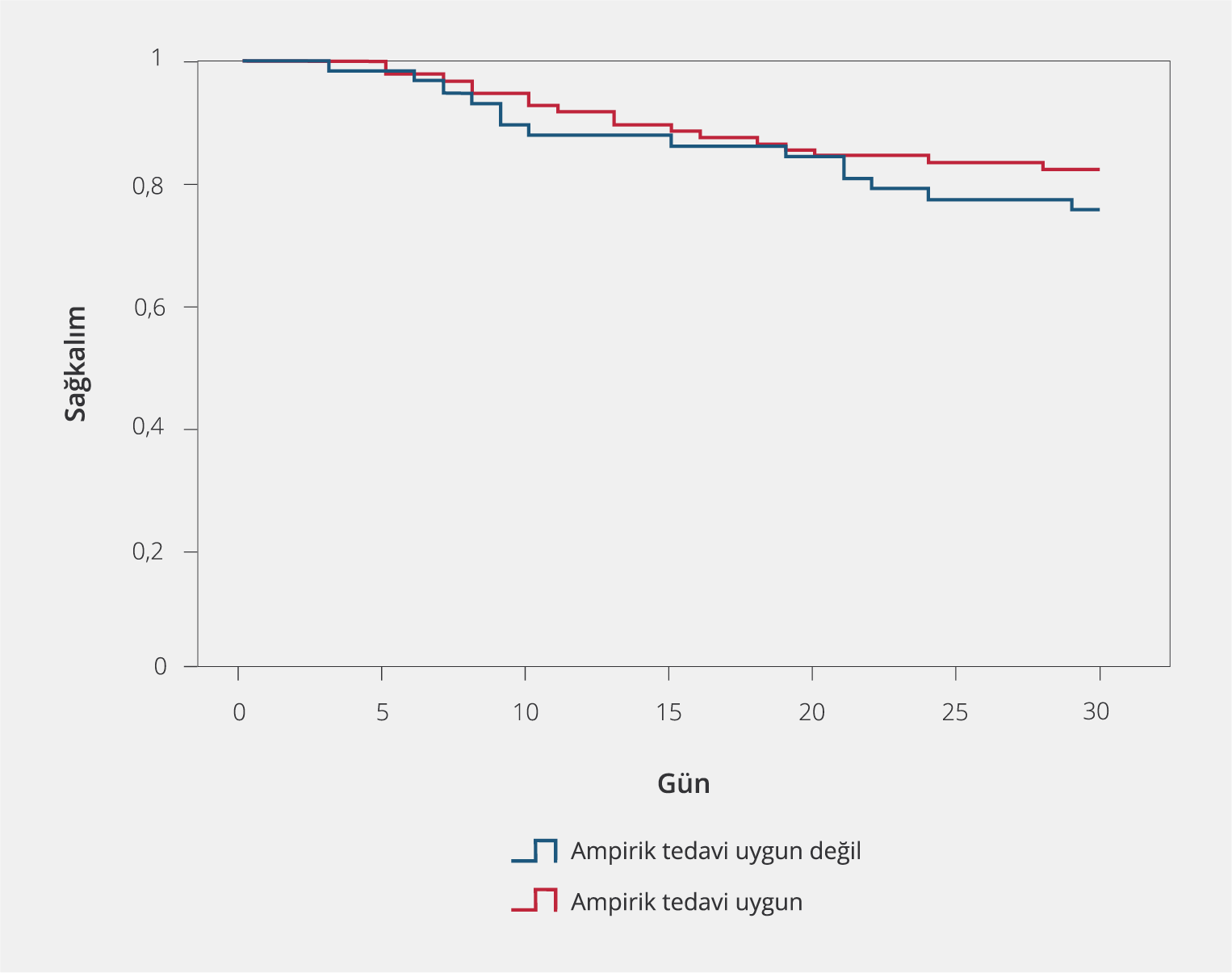
Hastalar, ampirik antibiyotik tedavisinin uygun olup olmamasına göre iki gruba ayrılarak hastanede yatış süresi, hastane yatışı sırasında gelişen mortalite ve 14, 30 ve 90 günlük tüm sebeplere bağlı mortalite sonuçları açısından karşılaştırıldılar. Bu parametreler arasında istatistiksel olarak anlamlı düzeyde fark saptanmadı. Ampirik antibiyotik tedavisinin uygunluğu ile sonuçlar arasındaki karşılaştırma, toplum kökenli infeksiyonlar, hastane kökenli infeksiyonlar ve üriner sistem infeksiyonları alt gruplarında da gerçekleştirildi. Bu alt gruplarda da hastalıkla ilgili sonuçlar ile ampirik antibiyotik tedavisi uygunluğu arasında istatistiksel olarak anlamlı düzeyde fark izlenmedi. Hastalığa ait sonuçlar ile ilgili değişkenler Tablo 2’de sunuldu. Tüm hastalar dahil edilerek gerçekleştirilen Kaplan-Meier sağkalım analizinde, ampirik antibiyotik tedavisi uygun olan ve olmayan hastalar arasında 30 günlük mortalite açısından anlamlı düzeyde fark saptanmadı (Şekil 2).
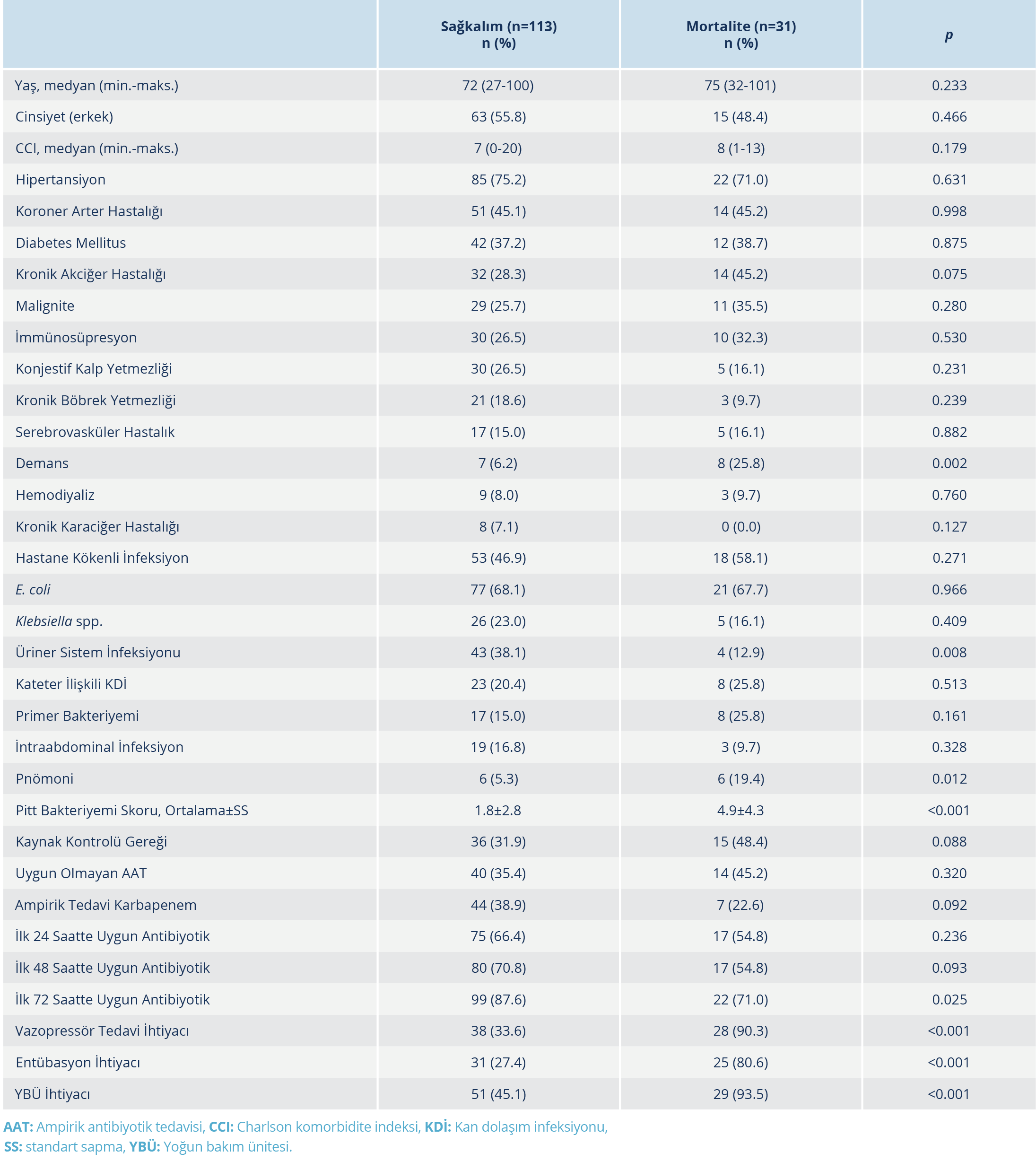
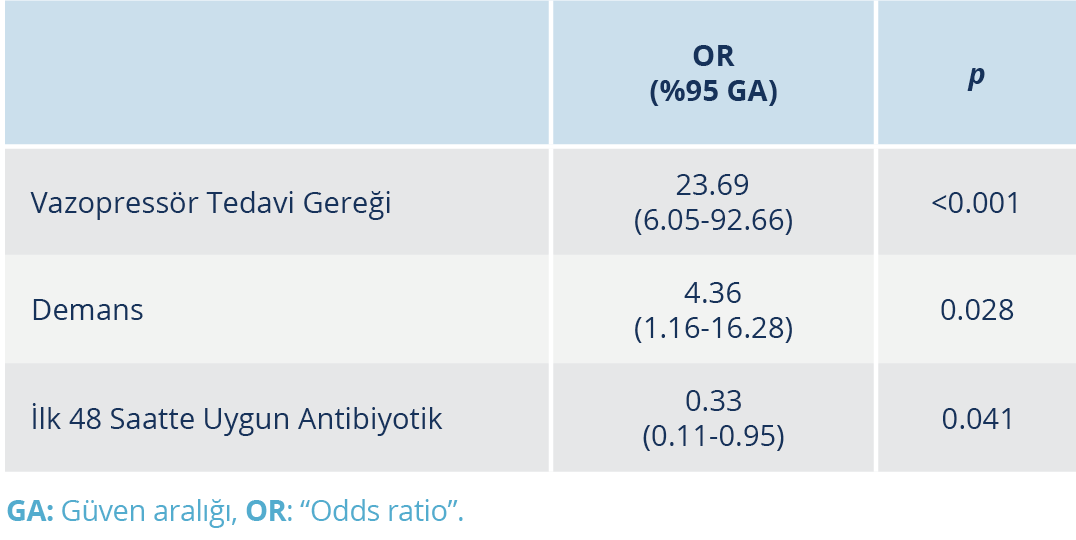
Çalışmada, hastaların 30 günlük tüm nedenlere bağlı mortalite oranı %21.5 (n=31) idi. Otuz günlük takipte mortalite gelişen ve gelişmeyen hastaların demografik ve klinik verilerinin karşılaştırılması Tablo 3’te sunuldu. Mortalite gelişen grupta anlamlı düzeyde daha yüksek bulunan değişkenler; demans varlığı, üriner sistem infeksiyonu dışı odaklara sekonder bakteriyemi, pnömoniye sekonder bakteriyemi, Pitt bakteriyemi skoru, vazopressör tedavi ihtiyacı, entübasyon gereksinimi ve yoğun bakım ünitesi yatış ihtiyacı iken etkene yönelik uygun antibiyotik tedavisinin 72 saatten önce başlanması sağ kalan grupta anlamlı düzeyde daha yüksek bulundu. Çok değişkenli lojistik regresyon analizine, p <0.100 olan değişkenler dahil edilmiş olup bu analizde demans varlığı ve vazopressör tedavi ihtiyacı, 30 günlük mortalite için bağımsız risk faktörleri olarak belirlendi. Ayrıca, etkene yönelik uygun antibiyotik tedavisinin 48 saatten önce başlanması mortaliteden koruyucu bir faktör olarak saptandı (Tablo 4).
İRDELEME
Çalışmamızda, üçüncü kuşak sefalosporin direnci gösteren Enterobacterales bakteriyemisinde ampirik antibiyotik tedavisinin mortalite ve hastane yatış süresi gibi klinik sonuçlara etkisi araştırıldı. Bu popülasyonda, uygun olmayan ampirik antibiyotik tedavisinin mortalite ve hastane yatışı üzerine herhangi bir olumsuz etkisi olmadığı saptandı. Otuz günlük mortalite için bu sonuç Kaplan-Meier sağkalım analizinde de gösterildi. Toplum kökenli, hastane kökenli ve üriner sistem infeksiyonuna sekonder gelişen bakteriyemide de ampirik antibiyotik tedavisi uygunluğunun mortalite artışı veya hastane yatış süresinin uzaması üzerine etkisi olmadığı tespit edildi. Çok değişkenli analizde, uygun antibiyotik tedavisine 48 saatten önce başlanmasının mortaliteden koruyucu faktör olduğu belirlendi.
Yapılan çalışmalarda, bakteriyemide uygun olmayan ampirik antibiyotik tedavisinin mortalite başta olmak üzere diğer olumsuz sonuçlar üzerine de etkisi olduğu bildirilmiştir (14,15). Ancak bu etki, infeksiyonun geliştiği ortam (toplum veya hastane), bakteriyeminin kaynağı, dahil edilen mikroorganizmaların türü ve direnç paternine bağlı olarak farklılık gösterebilmektedir. Ayrıca, uygun ampirik antimikrobiyal tedavisi tanımındaki farklılıklar (özellikle zamanlamasındaki) ve 30 günlük mortalite veya hastane yatışı sırasında gelişen mortalite gibi farklı klinik sonuçları tanımlayan değişkenlerin heterojenliği çalışmalarda farklı sonuçlara neden olmaktadır. Çalışmamızda belirli bir direnç paternine sahip etkenlerin dahil edilmesi, demografik ve klinik verilerin iki grup arasında DM dışında anlamlı fark göstermemesi, hastalığa ait sonuçları etkileyebilecek Charlson komorbidite indeksi, malignite, immünosüpresyon, kronik böbrek yetmezliği, hastane kökenli infeksiyon oranı, infeksiyon odaklarının dağılımı ve hastalık şiddeti değerlendirmede kullanılan Pitt bakteriyemi skoru değişkenlerinin iki grup arasında benzer özellik göstermesi çalışmanın sonuçlarının geçerliliği için önemli bulgulardır. Literatürde, özellikle toplum kökenli Gram-negatif bakteriyemide ve üriner sistem infeksiyonu kaynaklı bakteriyemide uygun olmayan ampirik antibiyotik tedavisinin mortalite artışı veya uzayan hastane yatış süresi ile ilişkili olmadığına dair benzer sonuçlar bildirilmiştir (12,16-18). Bu durum, toplum kökenli ve hastane kökenli bakteriyeminin virulans faktörleri açısından farklılık göstermesi, toplum kökenli bakteriyemide daha hafif klinik seyir gösteren üriner sistem infeksiyonlarının daha sık görülmesi, kaynak kontrolü gerektiren infeksiyonların daha nadir olması ve hastane kökenli infeksiyonlarda mortaliteye katkıda bulunabilecek ek faktörlerin (örneğin cerrahi müdahale, entübasyon, yabancı cisim varlığı, parenteral beslenme, vb.) daha az sıklıkta olması ile ilişkili olabilir.
Çalışmamızda, hastane kökenli bakteriyemide uygun olmayan ampirik antibiyotik tedavisi başlanan grupta mortalite oranı uygun tedavi alanlara göre daha yüksek olmasına rağmen, bu fark istatistiksel olarak anlamlı düzeyde değildi. Benzer direnç paternine sahip Enterobacterales bakteriyemisi için yapılan ve hasta popülasyonunun büyük çoğunluğunu (>%80) hastane kökenli infeksiyonların oluşturduğu iki çalışmada, ilk 24 saat içinde başlanan ampirik antibiyotik tedavisinin uygunluğu ile 30 günlük mortalite arasında bir ilişki saptanmadığı bildirilmiştir (11,19).
Bakteriyemisi olan hastalarda mortalite gelişimi sadece ampirik antibiyotik tedavisinin uygunluğu ile açıklanamayacak bir süreçtir. Mortaliteyi etkileyen faktörler; bakteriyeminin şiddeti (sepsis veya septik şok varlığı, yüksek Pitt bakteriyemi skoru), hasta komorbiditeleri (immünosüpresyon, malignite, DM, kronik böbrek yetmezliği, demans, vb.), kaynak kontrolünün zamanında yapılmaması, ampirik antibiyotik tedavisinden etkene yönelik kesin tedaviye geçiş süresi, antibiyotik tedavisi dışındaki destekleyici uygulamalar (sıvı replasmanı, oksijen desteği, vb.) ve bakteriyemi odağıdır.
Çalışmamıza, Enterobacterales takımından yalnızca üçüncü kuşak sefalosporin direnci gösteren bakterilerle gelişen bakteriyeminin dahil edilmiş olması, ilk 24 saat içerisinde hayatını kaybeden ve ek olarak karbapenem direnci gösteren hastaların hariç tutulması homojen bir grup için analiz yapılmasına olanak sağladı. Karıştırıcı faktörlerin etkisinin en aza indirilmesi için çok değişkenli lojistik regresyon analizi ve sonuçların geçerliliğini sağlayabilmek için ise Kaplan-Meier sağkalım analizi yapıldı. Elde edilen veriler ışığında, 30 günlük mortalite açısından bakteriyemi şiddeti, komorbid durumlar ve etkene yönelik tedavinin ne kadar erken başlandığı gibi değişkenlerin önemli olduğu düşünüldü. Amerikan İnfeksiyon Hastalıkları Derneği (IDSA)’nin 2024 yılı rehberinde GSBL üreten Enterobacterales infeksiyonlarının tedavisinde karbapenemler öncelikli olarak önerilmekte, ancak üriner sistem infeksiyonlarında florokinolonlar, trimetoprim-sulfametoksazol, piperasilin-tazobaktam gibi ajanların kullanımının düşünülebileceği belirtilmektedir. Rehberde, bu ajanların kullanımında infeksiyonun ciddiyeti, infeksiyon bölgesi, inokulum etkisi, sepsis varlığı gibi durumların göz önünde bulundurulması gerektiği de belirtilmiştir (9).
Çalışmamızda, kan kültürü alınması sonrası aynı gün içerisinde başlanan ampirik antibiyotik tedavisi uygunluğu, sonuçlarımızla anlamlı düzeyde ilişkili olmamakla birlikte 30 günlük mortalite için yapılan lojistik regresyon analizinde uygun antibiyotik tedavisinin 48 saatten önce başlanması mortalite için bağımsız bir koruyucu faktör olarak saptandı. Bu bulgu dahilinde, 3KSDE bakteriyemisi için kan kültürü alınması sonrasında ampirik antibiyotik tedavisine hemen başlanmasa bile, ilk 48 saat içerisinde başlanmasının sağkalıma katkı sağlayacağı belirlendi. Benzer özellikteki hastaları içeren çalışmalarda da etkene yönelik uygun antibiyotik tedavisinin, 72 saatten geç başlanmasının mortaliteyi artırdığı bildirilmiştir (13,20). Büyük çoğunluğunu bakteriyemi olgularının oluşturduğu ve Klebsiella pneumoniae ve E. coli infeksiyonlarını içeren bir sistematik derlemede, uygun antibiyotik tedavisindeki gecikmenin mortaliteyi artırdığı ve özellikle 48 saat ve üzerindeki gecikmede bu etkinin belirgin olduğu bildirilmiştir (21). Bu durum, infeksiyonun ilerlemesini sınırlamak için belirli bir zaman penceresi olduğunu düşündürmektedir. Bakteriyemi gibi ciddi infeksiyonlarda, özellikle üçüncü kuşak sefalosporin direnci gibi bir sorun olduğunda, ampirik tedavi uygun olmasa bile, etkene yönelik tedaviye mümkün olduğunca erken başlanması hayati önem taşımaktadır. Bu bulgu, hızlı tanı ve direnç belirleme testleri gibi yaklaşımların önemini desteklemektedir. Klinik uygulamada ampirik tedavinin yeterliliğine odaklanmaktan ziyade, gerekli olgularda hızlı bir şekilde uygun antibiyotik değişikliği daha kritik bir rol oynayabilir.
Çalışmamızda, vazopressör tedavi gereksinimi ve demans varlığı, mortaliteyle ilişkili faktörler olarak belirlendi. Yapılan diğer çalışmalarda da demans varlığının sepsis ve Gram-negatif etkenlere bağlı bakteriyemide artmış mortaliteyle ilişkili olduğu bildirilmiştir (22-24). Demans ile gelişen bilişsel bozukluk, eşlik eden beslenme yetersizliği ve immünolojik savunma mekanizmalarındaki eksiklikler bu ilişkiyi açıklayabilir. Ayrıca, septik şokun mortaliteyi artırdığı ve vazopressör tedavisi gereksiniminin kötü prognoz ile ilişkili olduğu önceki çalışmalarda da bildirilmiştir (25-27).
Retrospektif, gözlemsel nitelikte, tek merkezli olması ve sınırlı örneklem sayısı çalışmamızın kısıtlayıcı özellikleridir.
Çalışmamızda, 3KSDE bakteriyemisinde kan kültürü alındıktan sonra başlanan ampirik antibiyotik tedavisinin uygun olup olmamasının, mortalite ve hastane yatış süresi gibi sonuçlar üzerinde anlamlı bir etkisi saptanmadı. Buna karşın uygun antibiyotik tedavinin 48 saatten önce başlanması mortaliteden koruyucu bir faktör olarak belirlendi. Bu bulgular, yüksek riskli hasta grubunda kan kültürü alındıktan hemen sonra uygun antibiyotik tedavisine başlanmasa bile hedefe yönelik tedavinin mümkün olan en kısa sürede başlanmasının sağkalımı iyileştirmede kritik önem taşıdığını göstermektedir.
Hasta Onamı
Veriler retrospektif olarak değerlendirildiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma, Giresun Eğitim ve Araştırma Hastanesi Bilimsel Araştırmalar Etik Kurulu tarafından 18 Eylül 2024 tarih ve 18.09.2024/03 karar numarası onaylanmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman.
Yazar Katkıları
Fikir/Kavram – S.Ç., F.Ö.; Tasarım – S.Ç., F.Ö.; Denetleme – S.Ç.; Kaynak ve Fon Sağlama – S.Ç., F.Ö.; Malzemeler/Hastalar – S.Ç., F.Ö.; Veri Toplama ve/veya İşleme – S.Ç., F.Ö.; Analiz ve/veya Yorum – S.Ç., F.Ö.; Literatür Taraması – S.Ç., F.Ö.; Makale Yazımı – S.Ç.; Eleştirel İnceleme – S.Ç., F.Ö.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Referanslar
- Al-Hasan MN, Eckel-Passow JE, Baddour LM. Impact of healthcare-associated acquisition on community-onset Gram-negative bloodstream infection: a population-based study: healthcare-associated Gram-negative BSI. Eur J Clin Microbiol Infect Dis. 2012;31(6):1163-71. [CrossRef]
- Cetin S, Dokmetas I, Hamidi AA, Bayraktar B, Gunduz A, Sevgi DY. Comparison of risk factors and outcomes in carbapenem-resistant and carbapenem-susceptible Gram-negative bacteremia. Sisli Etfal Hastan Tip Bul. 2021;55(3):398-404. [CrossRef]
- Belley A, Morrissey I, Hawser S, Kothari N, Knechtle P. Third-generation cephalosporin resistance in clinical isolates of Enterobacterales collected between 2016-2018 from USA and Europe: Genotypic analysis of β-lactamases and comparative in vitro activity of cefepime/enmetazobactam. J Glob Antimicrob Resist. 2021;25:93-101. [CrossRef]
- Temkin E, Fallach N, Almagor J, Gladstone BP, Tacconelli E, Carmeli Y; DRIVE-AB Consortium. Estimating the number of infections caused by antibiotic-resistant Escherichia coli and Klebsiella pneumoniae in 2014: A modelling study. Lancet Glob Health. 2018;6(9):e969-79. [CrossRef]
- Bezabih YM, Sabiiti W, Alamneh E, et al. The global prevalence and trend of human intestinal carriage of ESBL-producing Escherichia coli in the community. J Antimicrob Chemother. 2021;76(1):22-9. [CrossRef]
- Woerther PL, Burdet C, Chachaty E, Andremont A. Trends in human fecal carriage of extended-spectrum β-lactamases in the community: Toward the globalization of CTX-M. Clin Microbiol Rev. 2013;26(4):744-58. [CrossRef]
- Paterson DL, Bonomo RA. Extended-spectrum beta-lactamases: a clinical update. Clin Microbiol Rev. 2005;18(4):657-86. [CrossRef]
- Bush K. Past and present perspectives on β-lactamases. Antimicrob Agents Chemother. 2018;62(10):e01076-18. [CrossRef]
- Tamma PD, Heil EL, Justo JA, Mathers AJ, Satlin MJ, Bonomo RA. Infectious Diseases Society of America 2024 Guidance on the treatment of antimicrobial-resistant Gram-negative infections. Clin Infect Dis. 2024:ciae403. [CrossRef]
- Xu S, Song Z, Han F, Zhang C. Effect of appropriate empirical antimicrobial therapy on mortality of patients with Gram-negative bloodstream infections: a retrospective cohort study. BMC Infect Dis. 2023;23(1):344. [CrossRef]
- Lim CL, Spelman D. Mortality impact of empirical antimicrobial therapy in ESBL- and AmpC-producing Enterobacteriaceae bacteremia in an Australian tertiary hospital. Infect Dis Health. 2019;24(3):124-33. [CrossRef]
- Joo EJ, Park DA, Lee NR, et al. Impact of appropriateness of empiric therapy on outcomes in community-onset bacteremia by extended-spectrum-β-lactamase producing Escherichia coli and Klebisella pneumoniae definitively treated with carbapenems. Eur J Clin Microbiol Infect Dis. 2017;36(11):2093-100. [CrossRef]
- Tumbarello M, Sanguinetti M, Montuori E, et al. Predictors of mortality in patients with bloodstream infections caused by extended-spectrum-beta-lactamase-producing Enterobacteriaceae: Importance of inadequate initial antimicrobial treatment. Antimicrob Agents Chemother. 2007;51(6):1987-94. Erratum in: Antimicrob Agents Chemother. 2007;51(9):3469. [CrossRef]
- Kadri SS, Lai YL, Warner S, et al; forming the National Institutes of Health Antimicrobial Resistance Outcomes Research Initiative (NIH-ARORI). Inappropriate empirical antibiotic therapy for bloodstream infections based on discordant in-vitro susceptibilities: a retrospective cohort analysis of prevalence, predictors, and mortality risk in US hospitals. Lancet Infect Dis. 2021;21(2):241-51. [CrossRef]
- Ohnuma T, Chihara S, Costin B, et al. Association of appropriate empirical antimicrobial therapy with in-hospital mortality in patients with bloodstream infections in the US. JAMA Netw Open. 2023;6(1):e2249353. [CrossRef]
- Nasomsong W, Changpradub D, Vasikasin V. Impact of inappropriate empirical antibiotic on outcomes in community-acquired third generation cephalosporin resistant Enterobacterales bacteremia. Infect Chemother. 2022;54(4):722-32. [CrossRef]
- Kang CI, Wi YM, Ko KS, et al. Outcomes and risk factors for mortality in community-onset bacteremia caused by extended-spectrum beta-lactamase-producing Escherichia coli, with a special emphasis on antimicrobial therapy. Scand J Infect Dis. 2013;45(7):519-25. [CrossRef]
- Dökmetaş İ, Hamidi AA, Bulut ME, Çetin S, Öncül A, Uzun N. Clinical effect of discordance in empirical treatment of cases with urinary tract infection accompanied by bacteremia. Turk J Urol. 2017;43(4):543-8. [CrossRef]
- Frakking FN, Rottier WC, Dorigo-Zetsma JW, et al. Appropriateness of empirical treatment and outcome in bacteremia caused by extended-spectrum-β-lactamase-producing bacteria. Antimicrob Agents Chemother. 2013;57(7):3092-9. [CrossRef]
- Anderson DJ, Engemann JJ, Harrell LJ, Carmeli Y, Reller LB, Kaye KS. Predictors of mortality in patients with bloodstream infection due to ceftazidime-resistant Klebsiella pneumoniae. Antimicrob Agents Chemother. 2006;50(5):1715-20. [CrossRef]
- Lodise TP, Zhao Q, Fahrbach K, Gillard PJ, Martin A. A systematic review of the association between delayed appropriate therapy and mortality among patients hospitalized with infections due to Klebsiella pneumoniae or Escherichia coli: How long is too long? BMC Infect Dis. 2018;18(1):625. [CrossRef]
- Chapelet G, Boureau AS, Dylis A, et al. Association between dementia and reduced walking ability and 30-day mortality in patients with extended-spectrum beta-lactamase-producing Escherichia coli bacteremia. Eur J Clin Microbiol Infect Dis. 2017;36(12):2417-22. [CrossRef]
- Maia MO, da Silveira CDG, Gomes M, et al. Multidrug-resistant bacteria on critically Ill patients with sepsis at hospital admission: risk factors and effects on hospital mortality. Infect Drug Resist. 2023;16:1693-704. [CrossRef]
- Rodríguez OL, Sousa A, Pérez-Rodríguez MT, et al. Mortality-related factors in patients with OXA-48 carbapenemase-producing Klebsiella pneumoniae bacteremia. Medicine (Baltimore). 2021;100(14):e24880. [CrossRef]
- Benetazzo L, Delannoy PY, Houard M, et al. Combination therapy with aminoglycoside in bacteremiasdue to ESBL-producing Enterobacteriaceae in ICU. Antibiotics (Basel). 2020;9(11):777. [CrossRef]
- Zohar I, Schwartz O, Yossepowitch O, David SSB, Maor Y. Aminoglycoside versus carbapenem or piperacillin/tazobactam treatment for bloodstream infections of urinary source caused by Gram-negative ESBL-producing Enterobacteriaceae. J Antimicrob Chemother. 2020;75(2):458-65. [CrossRef]
- Palacios-Baena ZR, Gutiérrez-Gutiérrez B, De Cueto M, et al; REIPI/ESGBIS/INCREMENT Group. Development and validation of the INCREMENT-ESBL predictive score for mortality in patients with bloodstream infections due to extended-spectrum-β-lactamase-producing Enterobacteriaceae. J Antimicrob Chemother. 2017;72(3):906-13. [CrossRef]