En Çok Okunanlar
Özet
Amaç: Yıllara göre antibiyotik direncindeki değişimleri incelemek, sürveyans çalışmaları aracılığıyla hastanelerin antibiyotik kullanım politikalarını düzenlemek ve ampirik tedavi protokollerini oluşturmak için kritik öneme sahiptir. Bu çalışmada, Hacettepe Üniversitesi Hastaneleri’nde 2010–2023 yılları arasında “SENTRY Antimicrobial Surveillance Program” kapsamında kullanılan Enterococcus faecium ve Enterococcus faecalis izolatlarının çeşitli antibiyotiklere karşı direnç profilleri, yıllara ve örnek türlerine göre karşılaştırıldı.
Yöntemler: Enterococcus spp. izolatları, 2010–2023 yılları arasında kan, solunum yolu, deri ve yumuşak doku, idrar, intraabdominal ve diğer steril vücut örneklerinden ardışık olarak izole edilmiş olup her hastadan tek bir örnek çalışmaya alındı. Ampisilin, piperasilin-tazobaktam, siprofloksasin, levofloksasin, linezolid, tigesiklin, teikoplanin, vankomisin duyarlılıkları Avrupa Antimikrobiyal Duyarlılık Testi Komitesi (EUCAST) kriterlerine uygun olarak mikrodilüsyon yöntemiyle değerlendirildi. Yüksek düzey aminoglikozid duyarlılığı ise disk difüzyon yöntemiyle belirlendi.
Bulgular: İzolatlar kan (n=161), solunum yolu (n=6), deri ve yumuşak doku (n=166), idrar (n=60), intraabdominal (n=80) ve diğer steril örneklerden (n=7) elde edilmişti. Toplam 480 Enterococcus spp. izolatı, E. faecium (n=241) ve E. faecalis (n=239) olarak tanımlandı. E. faecium izolatlarının; ampisilin, piperasilin-tazobaktam, siprofloksasin, levofloksasin, tigesiklin, teikoplanin, vankomisin direnç oranları sırasıyla %90.8, %93.6, %76.1, %80.4, %1.2, %20.3, %20.3 olarak belirlendi ve linezolid direnci saptanmadı. E. faecalis izolatlarında ise siprofloksasin, levofloksasin ve tigesiklin, direnç oranları sırasıyla %26.5, %22.3 ve %0.4, idi; ampisilin, piperasilin-tazobaktam, linezolid, teikoplanin ve vankomisin direnci ise saptanmadı. İncelenen tüm izolatların yıllara göre direnç dağılımında belirgin bir artış veya azalış belirlenemedi.
Sonuç: E. faecium izolatlarında antibiyotiklere karşı direnç, beklendiği üzere E. faecalis izolatlarına kıyasla daha yüksek bulundu. E. faecium izolatlarında vankomisin ve teikoplanin direnci tespit edilirken, E. faecalis izolatlarında direnç saptanmadı. Linezolid ve tigesiklinin her iki Enterococcus türüne karşı etkili olduğu in vitro olarak belirlendi.
Anahtar Kelimeler: Enterococcus faecium, Enterococcus faecalis, direnç, sürveyans
GİRİŞ
Enterococcus türleri birçok antibiyotiğe doğal dirençli olmaları, bu direnç genlerini transpozonlar aracılığıyla diğer bakterilere aktarabilmeleri, düşük ve yüksek sıcaklıklarda üreyebilmeleri ve hastane ortamlarında kolaylıkla yaşayabilmeleri nedeniyle hastane infeksiyonlarının başlıca etkenleri arasında yer almaktadır. İlk olarak 1980’li yıllarda bildirilen vankomisine dirençli enterokoklardan (VRE’ler) sonra günümüze kadar pek çok Enterococcus türü önemli nozokomiyal patojenler olarak bildirilmiştir (1-3). Enterokok kaynaklı hastane infeksiyonlarının sıklığı, vankomisin direncinin artışı ile paralel olarak artış göstermektedir. Enterokoklarda glikopeptit direncine yol açan 10 farklı gen kümesi (vanA, vanB, vanC, vanD, vanE, vanG, vanL, vanM, vanN ve vanP) tanımlanmış olup bu gen kümeleri arasından en sık olarak vanA saptanmaktadır; vanA geni hem vankomisin hem de teikoplanine karşı yüksek düzeyde dirence sebep olmaktadır (4). Hayvan yemlerinde avoparsinin yaygın kullanımının, VRE izolatlarının sıklığını artırdığı belirlenmiştir; bu nedenle Avrupa’da avoparsin kullanımı yasaklanmış ve bununla eş zamanlı olarak 2012–2017 yılları arasında VRE izolasyon sıklığında azalma gözlenmiştir (5).
Dünyada genelinde, hastane ve toplum kaynaklı infeksiyonlar sonucu elde edilen izolatlarda antibiyotik direnci endişe verici düzeyde artmaya devam etmektedir. Yıllara göre antibiyotik direncindeki değişimleri incelemek, sürveyans çalışmaları aracılığıyla hastanelerin antibiyotik kullanım politikalarının düzenlemek ve ampirik tedavi protokollerini oluşturmak için kritik öneme sahiptir. “SENTRY Antimicrobial Surveillance Program” 1997 yılından günümüze kadar hastane ve toplum kaynaklı infeksiyonlardan izole edilen etkenlerin incelendiği ve birçok merkezin katılım gösterdiği bir sürveyans programıdır. Ülkemizde iki merkez bu çalışmada yer almaktadır; Hacettepe Üniversitesi Hastaneleri bu merkezlerden biridir.
Bu çalışmada, Hacettepe Üniversitesi Hastaneleri’nde 2010–2023 yılları arasında “SENTRY Antimicrobial Surveillance Program” kapsamında Enterococcus faecium ve Enterococcus faecalis izolatlarının çeşitli antibiyotiklere karşı direnç profilleri, yıllara ve örnek türlerine göre karşılaştırılması amaçlandı.
YÖNTEMLER
Enterococcus spp. izolatları, 2010–2023 yılları arasında kan, solunum yolu, deri ve yumuşak doku, idrar, intraabdominal ve diğer steril vücut örneklerinden edilmiş olup her hastadan tek bir örnek çalışmaya alındı. Tüm etkenler, MALDI-TOF MS otomatize sistemi (Bruker Daltonics, Bremen, Almanya) ile tanımlandı ve sadece E. faecium ve E. faecalis izolatları çalışmaya alındı. Ampisilin, piperasilin-tazobaktam, siprofloksasin, levofloksasin, linezolid, tigesiklin, teikoplanin, vankomisin duyarlılıkları Avrupa Antimikrobiyal Duyarlılık Testi Komitesi (EUCAST) kriterlerine uygun olarak mikrodilüsyon yöntemiyle değerlendirildi. (6). Enterokoklarda vankomisin direnç tipi fenotipik olarak belirlendi (7). EUCAST kriterlerine göre, vanA tipi dirençte vankomisin ve teikoplanin minimal inhibitör konsantrasyonu (MİK) değerleri sırasıyla 64-1024 mg/lt ve 8-512 mg/lt, vanB tipi direçte ise sırasıyla 4-1024 mg/lt ve 0.06-1 mg/lt olması gerekmektedir (7). Yüksek düzey aminoglikozit direnci ise gentamisin (30 µg/ml) kullanılarak EUCAST kriterlerine uygun olarak belirlendi (6).
BULGULAR
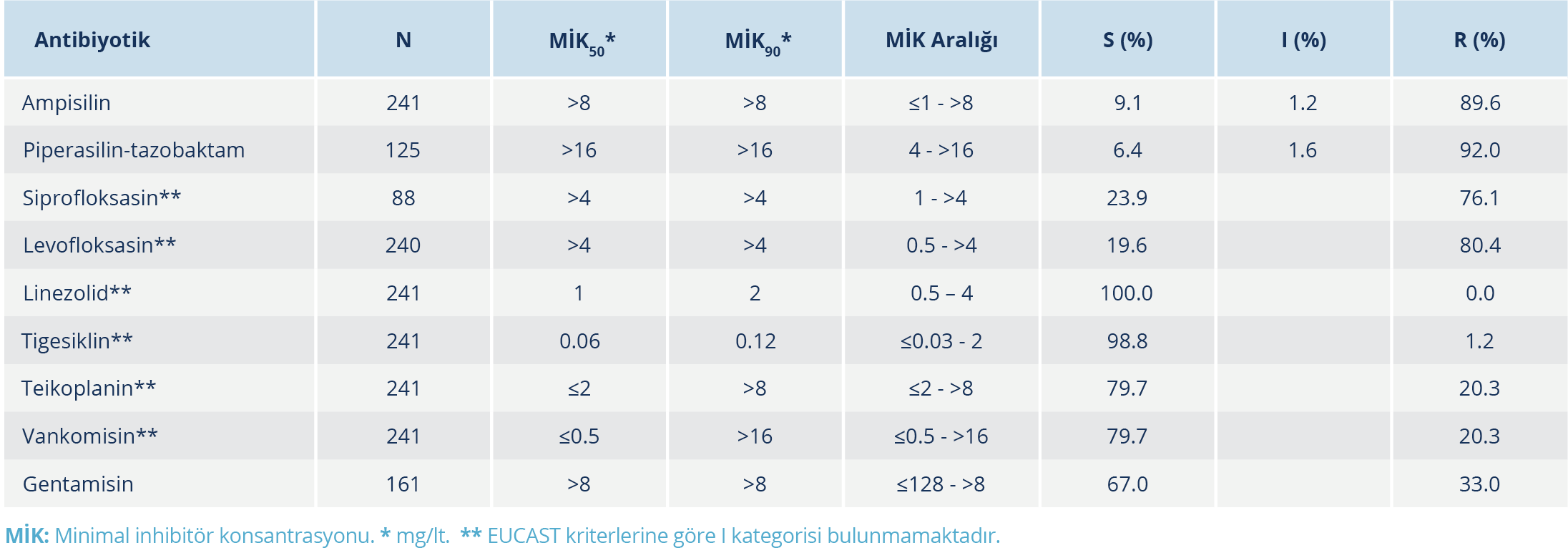
Tablo 1. Hacettepe Üniversitesi Hastanelerinde İzole Edilen E. faecium İzolatlarının Antibiyotik Duyarlılıkları (n=241)
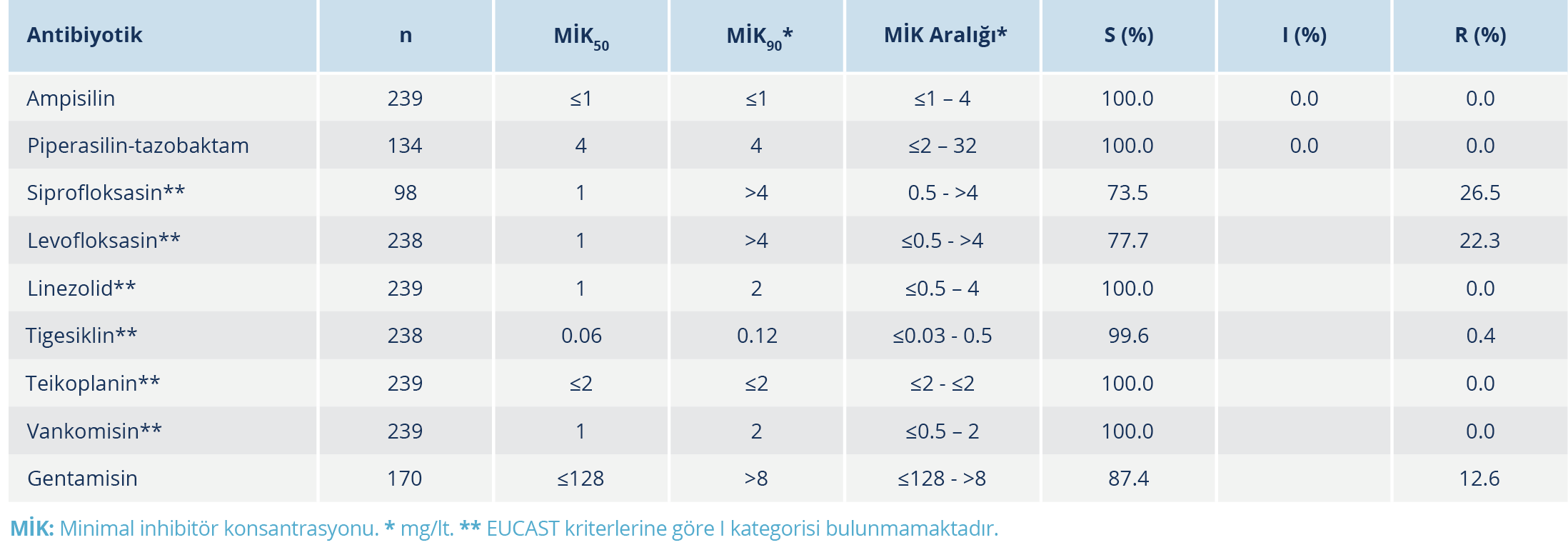
Tablo 2. Hacettepe Üniversitesi Hastanelerinde İzole Edilen E. faecalis İzolatlarının Antibiyotik Duyarlılıkları (n=239)
İzolatlar; kan (n=161), solunum yolu (n=6), deri ve yumuşak doku (n=166), idrar (n=60), intraabdominal (n=80) ve diğer steril örneklerden (n=7) elde edildi. Toplam 480 Enterococcus spp. izolatı MALDI-TOF MS otomatize sistemi (Bruker Daltonics, Bremen, Almanya) ile tanımlandı; izolatların dağılımı 214 E. faecium ve 239 E. faecalis şeklinde idi. İzolatların antibiyotik duyarlılıkları Tablo 1 ve 2’de verildi.
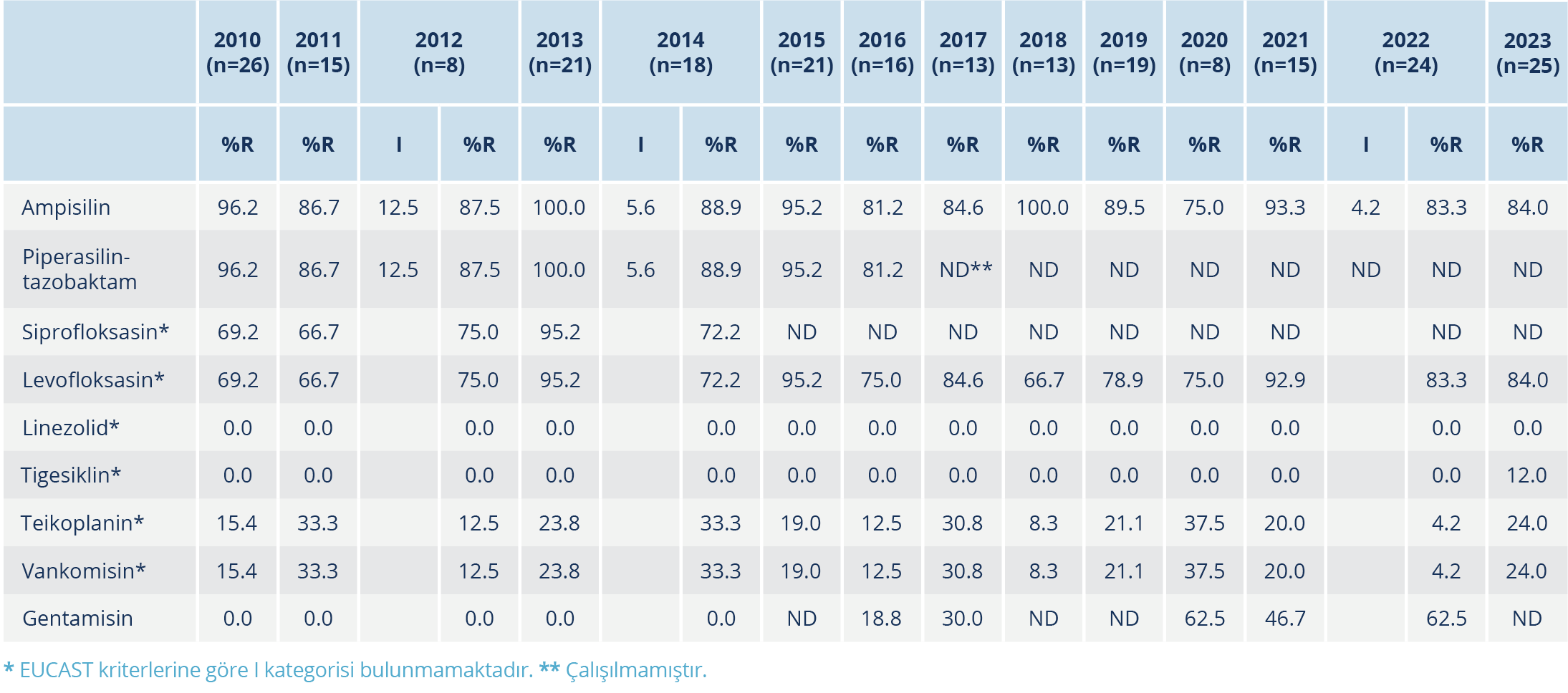
Tablo 4. Hacettepe Üniversitesi Hastanelerinde İzole Edilen E. faecium İzolatlarının Yıllara Göre Antibiyotik Duyarlılıkları
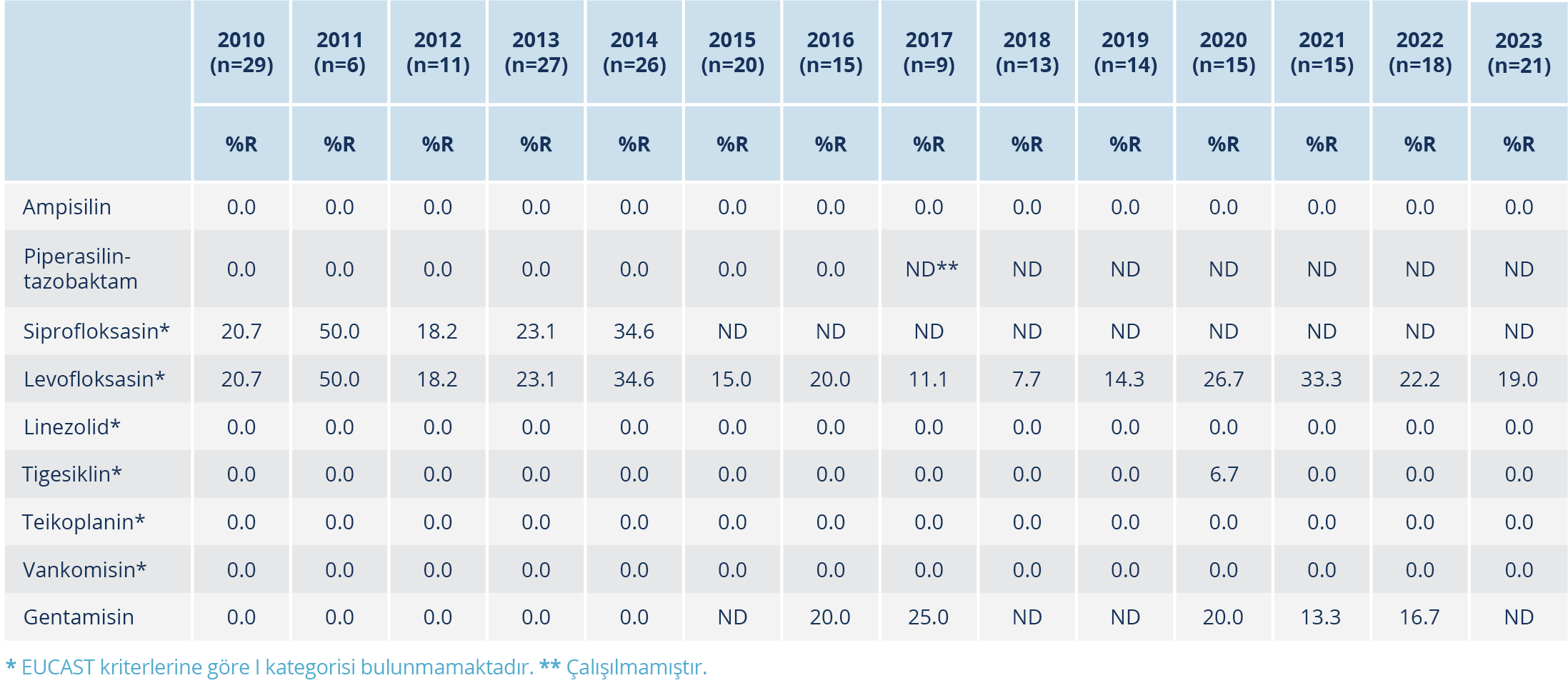
Tablo 5. Hacettepe Üniversitesi Hastanelerinde İzole Edilen E. faecalis İzolatlarının Yıllara Göre Antibiyotik Duyarlılıkları
E. faecium izolatlarının 49’u vankomisine dirençli bulundu. Vankomisine dirençli izolatlar kan (n=19), deri ve yumuşak doku (n=17), intraabdominal (n=10) ve idrar (n=3) örneklerinden izole edildi (Tablo 3). Vankomisine dirençli izolatların 46’sında vanA tipi, üçünde ise vanB tipi direnç belirlendi; vanA ve vanB tipi direnç tanımlanan izolatların direnç paternlerinde farklılık belirlenmedi. E. faecium ve E. faecalis izolatlarının yıllara göre duyarlılık sonuçları Tablo 4 ve Tablo 5’te verildi. Vankomisine dirençli E. faecium izolatlarının yıllara göre dağılımı incelendiğinde, belirgin bir artış veya azalış saptanmadı; E. faecalis izolatlarında ise vankomisin ve teikoplanin direnci saptanmadı.
Yüksek düzeyde gentamisin direnci, E. faecium izolatlarında %33, E. faecalis izolatlarında %12.6, vankomisine dirençli olan E. faecium’da ise %33.3 oranlarında belirlendi. Beklendiği gibi E. faecium izolatlarında antibiyotiklere karşı direnç E. faecalis’e göre daha yüksekti. Vankomisin ve teikoplanine karşı sadece E. faecium’da direnç saptandı. Linezolid ve tigesiklinin her iki enterokok türüne karşı etkili olduğu in vitro olarak saptandı.
İRDELEME
Enterokoklar, genellikle kan, cerrahi alan ve idrar yolu infeksiyonlarına neden olabilmekte ve birçok antibiyotiğe karşı direnç gösterebilmektedirler. Bu bakterilerin tür düzeyinde tanımlanmaları, uygun antibiyotik tedavisinin planlanması açısından son derece önemlidir. E. faecalis izolatları pek çok antibiyotiğe duyarlılık gösterirken, E. faecium izolatlarında daha yüksek oranda antibiyotik direnci ile karşılaşılabilmektedir. Çalışmamızda E. faecalis izolatlarının, E. faecium izolatlarına kıyasla daha duyarlı olduğu tespit edilmişti.
Normal mikrobiyotada ve çevrede yaygın olarak bulunan enterokoklar, hastane kaynaklı idrar yolu infeksiyonlarının etkenleri olarak ikinci sırada yer alırken, bakteriyemide üçüncü sıradadırlar (8-10). Çalışmamızda, 14 yıllık süreçte izole edilen enterokokların %33.5’i kan örneklerinden, %34.4’sı deri ve yumuşak doku örneklerinden, %1.3’ü solunum yolu örneklerinden, %1.4’ü diğer steril vücut örneklerinden ve %12.5’i de idrardan izole edildi.
Çalışmamızda ampisilin, piperasilin/tazobaktam direnci E. faecalis’te saptanmadı; E. faecium’da ise direnç oranları sırasıyla %89.6 ve %92 idi. Vankomisine dirençli enterokoklar ise bu antibiyotiklerin tümüne dirençli bulundu. Mert Dinç ve arkadaşlarının (11) çalışmasında, ampisilin direnci E. faecium ve E. faecalis için sırasıyla %89 ve %3 olarak bildirilmiştir (11). Bir diğer çalışmada ise ampisilin direnci E. faecium ve E. Faecalis için sırasıyla %96.3 ve %74 olarak tespit edilmiştir (12). Türkiye’nin de içinde olduğu uluslararası bir sürveyans çalışmasında, enterokok türlerinde ampisilin ve amoksasilin/klavulanik asit direnci sırasıyla %35.7 ve %35.8 olarak bildirilmiştir (13). Beta-laktam antibiyotiklere karşı direnç oranları değişiklik göstermektedir. Bu izolasyon bölgelerinin farklılığına, yoğun bakım etkeni olmalarına bağlı olarak da değişebilmektedir. Beta-laktam grubu ilaçlar dirençli enterokok infeksiyonlarının tedavisinde genellikle aminoglikozitler ile birlikte sinerjik etki için kullanılmaktadır. E. faecalis birçok beta-laktam ve karbapeneme, E. faecium’a kıyasla daha duyarlıdır. Bazı enterokoklarda beta-laktamaz enzim üretimi de bildirilmiştir; bu enzim beta-laktamaz inhibitörleri ile inhibe olmaktadır (14). E. faecium’da yüksek düzeyde ampisilin direnci için beta-laktamaz üretimi nadir olarak bildirilmekte olup direnç mekanizmasından en çok PBP5’in aşırı üretimi veya bu proteindeki mutasyonlar sorumlu tutulmaktadır (14). Çalışmamızda, E. faecium izolatlarında piperasilin-tazobaktam ile ampisilin direnç oranları arasında fark bulunmaması, bu izolatlardaki direncin beta-laktamaz üretimine bağlı olmadığını düşündürmektedir; ampisilin direncinin ise PBP5 mutasyonlarıyla açıklanabileceği değerlendirilmektedir.
Siprofloksasin ve levofloksasin direnci, sırasıyla E. faecium izolatlarında %76.1 ve %80.4; E. faecalis izolatlarında %26.5 ve %22.3; vankomisin dirençli enterokoklarda ise %100 olarak saptandı. Siprofloksasin ve levofloksasin direnç oranları ise birbirine yakındı. Sader ve arkadaşlarının (15) çalışmasında, florokinolon direnci E. faecium, E. faecalis ve vankomisin dirençli enterokoklar için sırasıyla %70, %33 ve %92 olarak bildirilmiştir. Savcı ve arkadaşlarının (16) çalışmasında, siprofloksasin direnci, E. faecium ve E. faecalis için %86 ve %45.3 olarak bildirilmiştir. Ülkemizde yapılan bir başka çalışmada ise siprofloksasin direnci, E. faecium ve E. faecalis için %86 ve %36 olarak bulunmuştur (17). Florokinolon direncinin diğer antibiyotiklere göre yüksek olması bu gruptaki antibiyotiklerin sıklıkla idrar yolu infeksiyonlarının tedavisinde kullanılmasından kaynaklanabilir.
Özellikle VRE infeksiyonlarının tedavisinde önemli bir seçenek olan linezolide karşı izolatlarımızda direnç belirlenmedi. Ancak, ülkemizde linezolid için düşük düzeylerde direnç bildiren çalışmalar da bulunmaktadır (16,17). Dünya Sağlık Örgütü (DSÖ)’nün Orta Asya ve Doğu Avrupa Antimikrobiyal Direnç Sürveyans (CAESAR) Ağı 2018 Raporu sonuçlarına göre ise ülkemizde linezolid direnci E. faecium izolatlarında %1 olarak bildirilmiştir (18). Linezolidin oldukça etkin olmasına karşın, uzun süreli linezolid tedavisi sonucunda linezolide dirençli enterokokların izole edildiği de bildirilmiştir (19,20). Çoklu direnç gösteren Gram-pozitif bakteri infeksiyonlarının tedavisinde önemli bir seçenek olan linezolidin gereksiz kullanımından kaçınılması gerekmektedir.
Çalışmamızda, tigesikline karşı E. faecium izolatlarında direnç %1.2,
E. faecalis izolatlarında % 0.4 olarak belirlendi; vankomisine dirençli
E. faecium izolatlarında ise tigesiklin direnci saptanmadı. “SENTRY Antimicrobial Surveillance Program”ın 1996-2016 yılları arasındaki sonuçlarında; VRE izolatlarında tigesiklin direnci Kuzey Amerika’da %0.8, Avrupa’da %0.5, Latin Amerika’da %0.7 ve Asya-Pasifik bölgesinde ise %0.6 olarak bildirilmiştir (21). Ülkemizde yapılan bir meta-analizi sonucuna göre E. faecium izolatlarında tigesiklin direnci % 0.2 olarak bulunmuştur (22). Çalışmamızda tigesiklinin, linezolidden sonra enterokok izolatlarına karşı en etkin antibiyotik olduğu görüldü. Bu sonuç, tigesiklinin klinik olarak kullanımı uygun olduğu durumlarda, tedavide dikkate alınması gereken bir alternatif olduğunu ortaya çıkarmaktadır.
Çalışmamız kapsamında, E. faecalis izolatlarının hiçbirinde teikoplanin ve vankomisin direnci saptanmadı. E. faecium izolatlarının %20.3’ünde ise vankomisin ve teikoplanin direnci birlikteliği mevcuttu. Vankomisin direnci, Kuzey Amerika’da %64.6, Afrika’da %28.6, Asya’da %22.8 ve Avrupa’da %17.7 oranlarında bildirilmiştir (23). Ülkemizde yapılan çalışmalarda vankomisin direnç oranları ortalama %10 civarındadır (13,24,25). Dünya Sağlık Örgütü’nün CEASAR 2018 sonuçlarına göre Türkiye’de vankomisin direnç oranı 2021 yılında %15.8 olup Ulusal Antimikrobiyal Direnç Sürveyans Sistemi (UAMDSS) 2016 Raporu’nda bu oran %16 olarak bildirilmiştir. Vankomisinin enterokoklara karşı hala en etkili antibiyotik olarak görülmesine karşın ülkemizde ve dünyada enterokoklarda vankomisin direnç oranlarının artışı endişe vericidir (16,19,26,27). Vankomisin direncindeki artışın en önemli nedenleri uzun süre yoğun bakımda kalma ve uzun süreli kullanımdır. Vankomisine dirençli enterokoklar çoğunlukla sağlıklı kişilerin gastrointestinal sisteminde kolonize olmakta, sağlık personeli aracılığı ile hastaya bulaşmaktadır; korunma önlemlerine dikkat edilmesi VRE aracılığı ile gelişen infeksiyonlarda azalma sağlayabilir. Vankomisin direncine neden olan gen kümeleri arasında en yaygın görüleni VanA tipi direnç genidir (4). Bizim çalışmamızda da VanA tipi direnç geni yaygın olarak saptandı.
Çalışmamızda, E. faecium izolatlarında antibiyotiklere direnç, E. faecalis’e göre daha yüksek bulundu. Yıllar içinde antibiyotik direncinde belirgin artış ya da azalış saptanmadı. Linezolid ve tigesiklin her iki enterokok türünde de en etkili antibiyotikti. Sonuç olarak; uygun ampirik antibiyotik tedavisi için tür tayinin doğru bir şekilde yapılması oldukça önemlidir.
Hasta Onamı
N.A.
Etik Kurul Kararı
Çalışmada sürveyans programı kapsamındaki izolatlar kullanıldığı için etik kurul onayı alınmamıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman.
Yazar Katkıları
Fikir/Kavram – B.A., G.H., D.G.; Tasarım – B.A., G.H., D.G.; Denetleme – B.A., G.H., D.G.; Kaynak ve Fon Sağlama – B.A., G.H., D.G.; Malzemeler/Hastalar – B.A., G.H., D.G.; Veri Toplama ve/veya İşleme – B.A., G.H., D.G.; Analiz ve/veya Yorum – B.A., G.H., D.G.; Literatür Taraması – B.A., G.H., D.G.; Makale Yazımı – B.A., G.H., D.G.; Eleştirel İnceleme – B.A., G.H., D.G.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Bilimsel Etkinlik
Bu çalışma 9-11 Mayıs 2024 tarihleri arasında İstanbul’da, Marmara Üniversitesi Pendik Eğitim ve Araştırma Hastanesi’den düzenlenen 15. Antimikrobik Kemoterapi Günleri’nde poster olarak sunulmuştur.
Referanslar
- Leclercq R, Derlot E, Duval J, Courvalin P. Plasmid-mediated resistance to vancomycin and teicoplanin in Enterococcus faecium. N Engl J Med. 1988;319(3):157-61. [CrossRef]
- Uttley AH, George RC, Naidoo J, et al. High-level vancomycin-resistant enterococci causing hospital infections. Epidemiol Infect. 1989;103(1):173-81. [CrossRef]
- Ramos S, Silva V, Dapkevicius MLE, Igrejas G, Poeta P. Enterococci, from harmless bacteria to a pathogen. Microorganisms. 2020;8(8):1118. [CrossRef]
- Al Rubaye M, Janice J, Bjørnholt JV, et al, The Norwegian Vre Study Group. The population structure of vancomycin-resistant and -susceptible Enterococcus faecium in a low-prevalence antimicrobial resistance setting is highly influenced by circulating global hospital-associated clones. Microb Genom. 2023;9(12):001160. [CrossRef]
- Miller WR, Murray BE, Rice LB, Arias CA. Resistance in vancomycin-resistant enterococci. Infect Dis Clin North Am. 2020;34(4):751-71. [CrossRef]
- Breakpoint tables for interpretation of MICs and zone diameters; version 14.0 [Internet]. In: The European Committee on Antimicrobial Susceptibility Testing (EUCAST) web site; January 1, 2024. [erişim 3 Eylül 2024]. https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Breakpoint_tables/v_14.0_Breakpoint_Tables.pdf
- The EUCAST guideline on detection of resistance mechanisms; v 2.0 [Internet]. In: The European Committee on Antimicrobial Susceptibility Testing (EUCAST) web site; July 11, 2017. [erişim 3 Eylül 2024]. https://www.eucast.org/resistance_mechanisms
- Desai PJ, Pandit D, Mathur M, Gogate A. Prevalence, identification and distribution of various species of enterococci isolated from clinical specimens with special reference to urinary tract infection in catheterized patients. Indian J Med Microbiol. 2001;19(3):132-7.
- Vehreschild MJGT, Haverkamp M, Biehl LM, Lemmen S, Fätkenheuer G. Vancomycin-resistant enterococci (VRE): a reason to isolate? Infection. 2019;47(1):7-11. [CrossRef]
- Paul M, Nirwan PS, Srivastava P. Isolation of Enterococcus from various clinical samples and their antimicrobial susceptibility pattern in a tertiary care hospital. Int J Curr Microbiol App Sci. 2017;6(2):1326-32. [CrossRef]
- Mert Dinç B, Karabiber N, Aykut Arca E. [Macrolide – lincosamide – streptogramin B (MLSB) resistance and fusidic acid susceptibility of methicillin resistant Staphylococcus aureus (MRSA) strains isolated from clinical samples]. Turk Hij Den Biyol Derg. 2009;66(3):89-94. Turkish.
- Etiz P, Kibar F, Ekenoğlu Y, Yaman A. [Evaluation of the antibiotic resistance profiles of Enterococcus species ısolated from urine cultures]. Türk Mikrobiyol Cem Derg. 2014;44(3):107-13. Turkish. [CrossRef]
- Jones RN, Flonta M, Gurler N, Cepparulo M, Mendes RE, Castanheira M. Resistance surveillance program report for selected European nations (2011). Diagn Microbiol Infect Dis. 2014;78(4):429-36. [CrossRef]
- García-Solache M, Rice LB. The Enterococcus: a model of adaptability to its environment. Clin Microbiol Rev. 2019;32(2):e00058-18. [CrossRef]
- Sader HS, Watters AA, Fritsche TR, Jones RN. Daptomycin antimicrobial activity tested against methicillin-resistant staphylococci and vancomycin-resistant enterococci isolated in European medical centers (2005). BMC Infect Dis. 2007;7:29. [CrossRef]
- Savcı Ü, Şahin M, Eser B. [The evaluation of antimicrobial resistances of Enterococcus faecalis and Enterococcus faecium strains isolated from clinical specimens]. J Health Sci Med 2018;1(1):4-8. Turkish. [CrossRef]
- Ödemiş İ, Köse Ş, Ersan G, Çelik D, Akbulut İ. [Evaluation of antibiotic susceptibilities of enterococcus strains isolated from clinical samples of hospitalized patients]. Turk Hij Den Biyol Derg. 2018;75(4):345-52. Turkish. [CrossRef]
- Antimicrobial resistance surveillance in Europe 2023 – 2021 data [Internet]. Stockholm: European Centre for Disease Prevention and Control and World Health Organization; 2023. [erişim 3 Eylül 2024]. https://www.ecdc.europa.eu/sites/default/files/documents/Antimicrobial%20resistance%20surveillance%20in%20Europe%202023%20-%202021%20data.pdf
- Auckland C, Teare L, Cooke F, Kaufmann ME, Warner M, Jones G, et al. Linezolid-resistant enterococci: report of the first isolates in the United Kingdom. J Antimicrob Chemother. 2002;50(5):743-6. [CrossRef]
- Swoboda S, Fritz S, Martignoni ME, et al. Varying linezolid susceptibility of vancomycin-resistant Enterococcus faecium isolates during therapy: a case report. J Antimicrob Chemother. 2005;56(4):787-9. [CrossRef]
- Pfaller MA, Cormican M, Flamm RK, Mendes RE, Jones RN. Temporal and geographic variation in antimicrobial susceptibility and resistance patterns of enterococci: results from the SENTRY Antimicrobial Surveillance Program, 1997-2016. Open Forum Infect Dis. 2019;6(Suppl 1):S54-S62. [CrossRef]
- Kilbas I, Ciftci IH. Antimicrobial resistance of Enterococcus isolates in Turkey: A meta-analysis of current studies. J Glob Antimicrob Resist. 2018;12:26-30. [CrossRef]
- Seifert H, Blondeau J, Dowzicky MJ. In vitro activity of tigecycline and comparators (2014-2016) among key WHO ‘priority pathogens’ and longitudinal assessment (2004-2016) of antimicrobial resistance: a report from the T.E.S.T. study. Int J Antimicrob Agents. 2018;52(4):474-84. [CrossRef]
- Sig AK, Kula Atik T, Çetin Duran A. Antibiotic resistance of Enterococcus species: 3-year data. J Health Sci Med. 2021;4(5):670-4. [CrossRef]
- Gedik T, Kiraz N, Duran H. The change of antibiotic resistance rates over the years in Enterococcus spp. isolated from clinical specimens. J Health Sci Med. 2023;6(5):1052-8. [CrossRef]
- Altun B, Cengiz AB, Kara A, et al. First vancomycin-resistant blood isolate of Enterococcus faecium in a children’s hospital and molecular analysis of the mechanism of resistance. Turk J Pediatr. 2008;50(6):554-8.
- Mendes RE, Castanheira M, Farrell DJ, Flamm RK, Sader HS, Jones RN. Longitudinal (2001-14) analysis of enterococci and VRE causing invasive infections in European and US hospitals, including a contemporary (2010-13) analysis of oritavancin in vitro potency. J Antimicrob Chemother. 2016;71(12):3453-8. [CrossRef]