En Çok Okunanlar
Özet
Amaç: Solunum yolu infeksiyonları tüm dünyada önemli bir halk sağlığı sorunudur. Günümüzde kullanılan moleküler tabanlı solunum yolu paneli ile etkenler kısa sürede yüksek duyarlılık ile belirlenebilmektedir. Çalışmamızın amacı testin pozitifliği ile hastanın demografik verileri, şikâyet ve semptomları, komorbiditeleri ve başlangıç laboratuvar parametreleri arasındaki ilişkiyi belirleyerek testin akılcı bir şekilde kullanımına katkıda bulunmaktır.
Yöntemler: Eylül 2023–Nisan 2024 tarihleri arasında solunum yolu paneli istemi olan 915 örnek çalışmaya dahil edildi. Örnekler Qiagen® QIAstat-Dx Analyzer 1.0 (Qiagen, Almanya) cihazında QIAstat-Dx® Respiratory SARS-CoV-2 panel kiti (Qiagen, Almanya) ile çalışıldı. Örneklerin hangi kliniklerden geldiği, hastaların epidemiyolojik özellikleri, istem anındaki şikayetleri, lökosit sayıları ve C-reactive protein (CRP) değerleri, o dönemde sahip oldukları ek hastalıklar retrospektif olarak hasta dosyalarından elde edildi.
Bulgular: Çalışmaya dahil edilen 915 örneğin 559 (%61.09)’u pozitifti. Cinsiyet ve hastaların yattığı bölüm açısından pozitif ve negatif hastalar arasında anlamlı düzeyde bir fark saptanmadı. Ancak, öksürük, burun akıntısı, balgam ve boğaz ağrısı varlığı ile ≤18 yaş olan hasta grubunda pozitiflik açısından istatistiksel olarak anlamlı düzeyde bir fark olduğu görüldü (p<0.05). Panel negatif grupta ek hastalık varlığı istatistiksel olarak anlamlıydı (p<0.05). CRP değerleri ve lökosit sayıları için alıcı işletim karakteristiği eğrisi (Receiver Operating Characteristic Curve – ROC)’nde güvenilir ve ayırt edici bir kesim noktası belirlenemedi. Ki-kare otomatik etkileşim (Chi-square Automatic Interaction Detection – CHAID) algoritması sonuçlarına göre, panelin pozitif veya negatif olmasını en çok etkileyen değişkenler sırasıyla öksürük, yaş, ek hastalık ve dispne olarak belirlendi.
Sonuç: Solunum yolu infeksiyonlarında klinik bulguların varlığında, panelin akılcı kullanımı sayesinde etkenin kısa sürede tespit edilmesi, uygun tedaviye zamanında başlanması ve böylece sağlık harcamalarının ekonomiye olan yükünün azaltılması mümkün olacaktır.
GİRİŞ
Solunum yolu infeksiyonları (SYİ’ler) dünya çapında önemli bir halk sağlığı sorunudur; hızlı ve kolay bulaşmaları nedeniyle hem hastaneye yatışlardan hem de ölümlerden önemli derecede sorumludurlar. Bu durum, küresel olarak sağlık sistemleri üzerinde hem tıbbi hem de ekonomik açıdan büyük yük oluşturmaktadır (1,2).
Çeşitli bakteri ve virusların etken olduğu SYİ’lerin benzer semptomlarla seyretmeleri nedeniyle tanılarında zorluk yaşanmaktadır. Bu durum, antibiyotiklerin gereksiz bir şekilde reçetelendirilmesine ve buna bağlı olarak antibiyotik dirençli suşların ortaya çıkmasına neden olmaktadır (3). Ülkemiz antibiyotik kullanımının ve buna bağlı olarak antimikrobiyal direncin yüksek olduğu ülkeler arasındadır (4). Amerika Birleşik Devletleri (ABD) ve Kanada gibi gelişmiş ülkelerde de antibiyotik reçetelerinin %30-50’sinin uygun olmadığı tahmin edilmektedir. Ayrıca, tüm antibiyotik reçetelerinin yaklaşık %50’sinin üst solunum yolu infeksiyonları için yazılması, bu tür infeksiyonlarda uygunsuz antibiyotik kullanımının yüksek olduğunu göstermektedir (5).
Uygun ve etkin tedavi için hızlı ve kesin tanı testlerine ihtiyaç vardır. Geleneksel kültür tabanlı yöntemler, yetkin personel ihtiyacı ve uzun işlem süreleri nedeniyle sınırlı kalmaktadır. Buna karşılık, multipleks polimeraz zincir reaksiyonu (PCR) teknikleri solunum yolu patojenlerini tanımlamada yüksek doğruluk ve hız sağlamaktadır (3). Benzer şekilde, nükleik asit amplifikasyon testleri de SYİ etkenlerinin tespiti için en hassas yöntemler olarak kabul edilmektedir (6). Günümüzde SYİ etkenlerini aynı anda tespit etmeye yönelik sendromik panel testleri kullanılmaktadır. Söz konusu testler sayesinde üst SYİ etkenlerinin kısa sürede tespiti mümkün olmaktadır; bu durum antimikrobiyal veya antiviral tedavinin zamanında ve uygun şekilde verilmesine olanak sağlayarak antimikrobiyal yönetimini kolaylaştırmaktadır (7).
Çalışmamızın amacı, solunum yolu paneli sonuçları ile hastaların demografik verileri, şikayet ve semptomları, eşlik eden hastalıkları ve başlangıç laboratuvar parametreleri arasındaki ilişkiyi değerlendirmek, ki-kare otomatik etkileşim (Chi-Square Automatic Interaction Detection – CHAID) algoritmasını kullanarak SYİ’lere etki eden faktörleri belirlemek ve böylece klinisyenlere tanı süreci için destek sunmaktır. Ayrıca moleküler testlerin daha bilinçli bir şekilde kullanımının geliştirilmesi, etkin tedavinin kısa sürede uygulanması ve bu şekilde ekonomiye olan yükün azaltılması hedeflenmektedir.
YÖNTEMLER
Çalışma retrospektif olarak gerçekleştirildi ve Eylül 2023–Nisan 2024 tarihleri arasında mikrobiyoloji laboratuvarına solunum yolu paneli istemi ile gönderilen toplam 915 örnek çalışmaya dahil edildi. Hastaların epidemiyolojik özellikleri, istem anındaki vital bulguları, şikayetleri, lökosit sayıları, C-reaktif protein değerleri ve sahip oldukları ek hastalıklar (hipertansiyon, diabetes mellitus, kronik obstrüktif akciğer hastalığı, akut-kronik böbrek yetmezliği, malignite, immün sistem hastalıkları) hasta dosyalarından elde edildi.
Farklı yaş gruplarını ve tüm ili kapsayan örnekler nasofarengeal sürüntü yöntemiyle alınarak naSTM® numune taşıma ortamında (MAYGEN Laboratuvar Hizmetleri Ltd. Şti, Türkiye) laboratuvara gönderildi. Gönderilen örnekler Qiagen®QIAstat-Dx analyzer 1.0 (Qiagen, Almanya) cihazında QIAstat-Dx® Respiratory SARS-CoV-2 panel kiti (Qiagen, Almanya) ile çalışıldı. Bu kit; rhinovirus/enterovirus, solunum sinsityal virusu (RSV) A/B, SARS-CoV-2, influenza A, influenza A subtip H1, influenza H1N1/2009, influenza A subtip H3, influenza B, parainfluenza virus (PIV) 1, PIV 2, PIV 3, PIV 4, human coronavirus (HCoV) OC43, HCoV NL63, HCoV HKU1, HCoV 229E, adenovirus, Bordetella pertussis, Mycoplasma pneumoniae, human metapneumovirus (HMPV) A/B, Legionella pneumophilla, human bocavirus (HBoV) etkenlerini yaklaşık 69 dakikada tespit etmekte idi.
Çalışma için Giresun Eğitim ve Araştırma Hastanesi Bilimsel Araştırmalar Etik Kurulu’ndan 6 Kasım 2023 tarih ve 06.11.2023/10 karar numarasıyla onay alındı.
İstatistiksel Analizler
Verilerin analizi, SPSS (Statistical Package for the Social Sciences) versiyon 20.0 programı (IBM Corp., Armonk, NY, ABD) ile yapıldı. Etken durumu ile birlikte hastaların yaş grupları, cinsiyetleri, klinik bulguları, yattıkları servis, ek hastalık varlığı arasındaki ilişki için Phi katsayısı ve p değeri, CRP ve lökosit değerleri için alıcı işletim karakteristiği eğrisi (Receiver Operating Characteristic Curve – ROC) kullanıldı. Ayrıca, panel istemini etkileyen faktörleri analiz etmek için CHAID algoritması uygulandı; CHAID kategorik değişkenler arasındaki anlamlı etkileşimleri belirleyerek veri kümelerini segmentlere ayıran ve karar ağacı tekniğine dayanan bir makine öğrenmesi sınıflandırma yöntemidir. (8,9).
BULGULAR
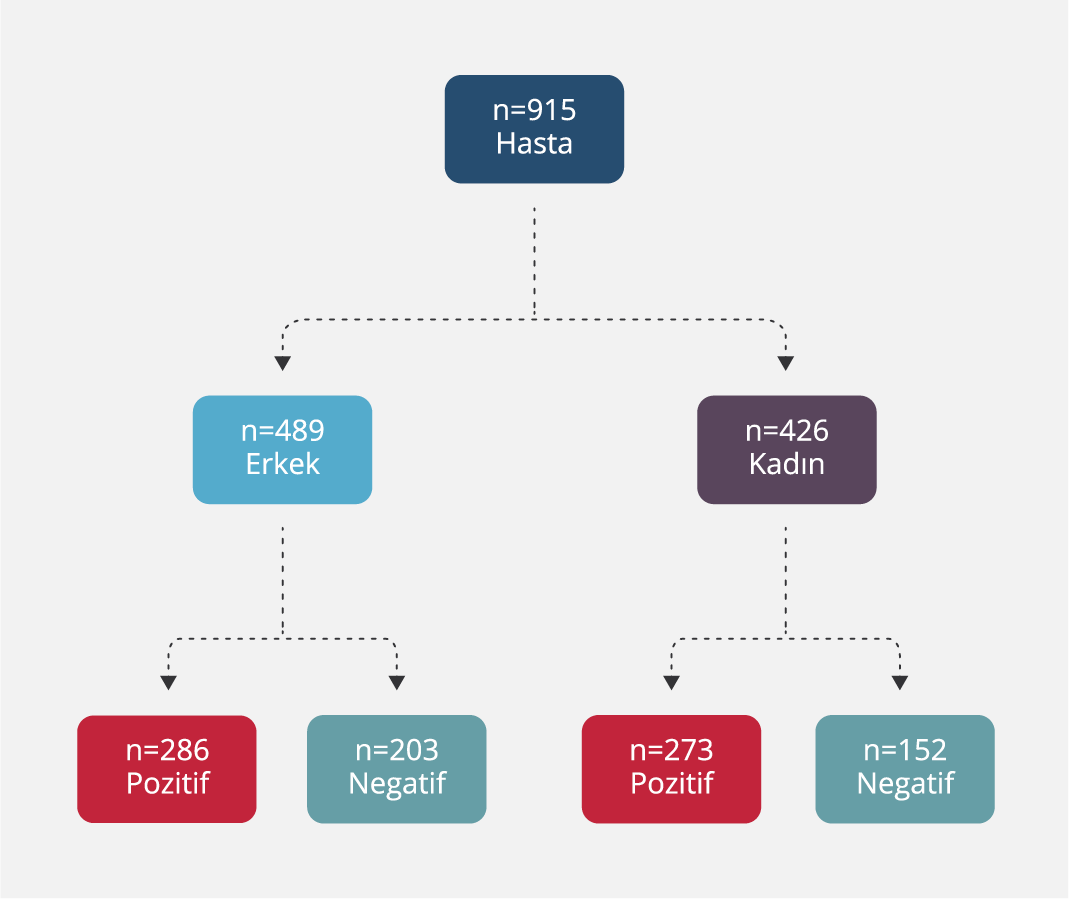
Laboratuvara solunum yolu paneli istemi ile gönderilen 915 örneğin 559 (%61.09)’unun test sonucu pozitif olup toplam 689 etken tespit edilmişti. Hastaların genel yaş ortalaması 40.24 (±33.82) ve pozitif hastaların yaş ortalaması 30.77 (±33.37) yıl idi. Hastaların cinsiyete göre dağılımları Şekil 1’de sunuldu. Erkek hastaların %58.48’inde, kadın hastaların ise %64.08’inde en az bir etken pozitif olarak tespit edilmişti. Cinsiyete göre değerlendirildiğinde pozitif ve negatif hasta grupları arasında istatistiksel olarak anlamlı bir fark bulunmadı.
Yaş gruplarına göre analiz edildiğinde, 0 yaş, 1-18 yaş, 19-65 yaş ve 65 yaş üstü kategorilerine ayrılan örneklerin pozitiflik oranları sırasıyla %89.70, %76.5, %52.6 ve %43.70 olarak tespit edildi. Pozitif ve negatif hasta grupları yaşa göre değerlendirildiğinde, ≤18 yaş olan grupta pozitiflik oranının istatistiksel olarak anlamlı düzeyde yüksek olduğu görüldü (p<0.05).
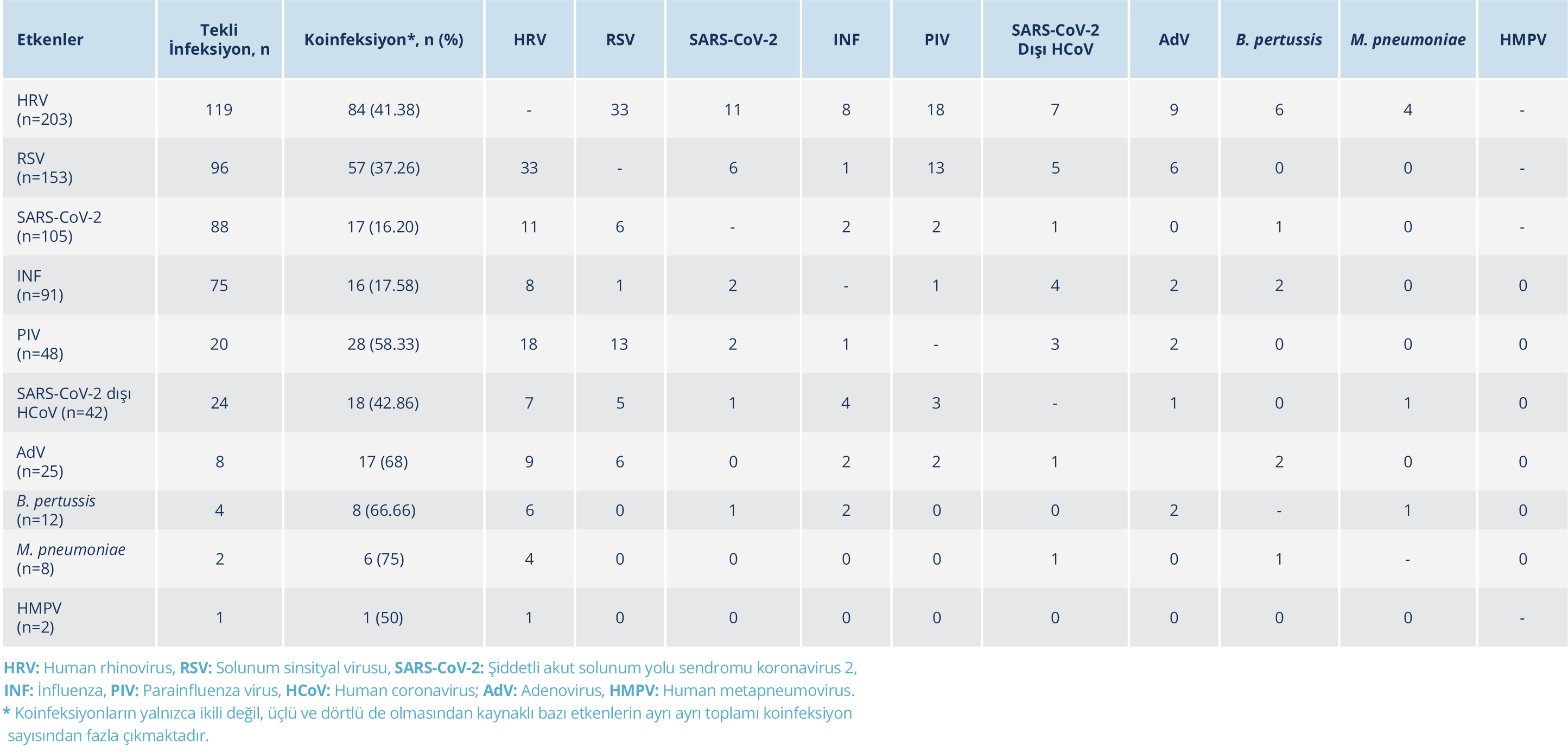
Örnekler kaynakları açısından değerlendirildiğinde, 915 örneğin 564’ü servis, 212’si yoğun bakım, 139’u poliklinik hastalarına ait olduğu görüldü; pozitiflik oranları sırasıyla %60.46, %59.43 ve %66.18 idi. Hastaların yattığı bölüm ve etken arasında istatistiksel olarak anlamlı bir ilişki yoktu. Pozitif hastalara bakıldığında, en sık olarak human rhinovirus (HRV) (%36.31) tespit edilirken, L. pneumophilla ve HBoV hiç tespit edilmemişti. Bakteri ve virusun birlikte etken oldukları infeksiyon durumu 12 hastada, yalnızca bakteriyel infeksiyon ise yedi hastada tespit edilirken, 540 (%96.6) hastada tekli veya çoklu viral etkenler görüldü. Pozitiflik tespit edilen 559 hastanın %21.82’sinde iki veya daha fazla etken birlikte idi; en sık olarak HRV-RSV birlikteliği tespit edildi. Solunum yolu infeksiyon etkenlerinin tekli ve koinfeksiyonlardaki dağılımı Tablo 1’de sunuldu.
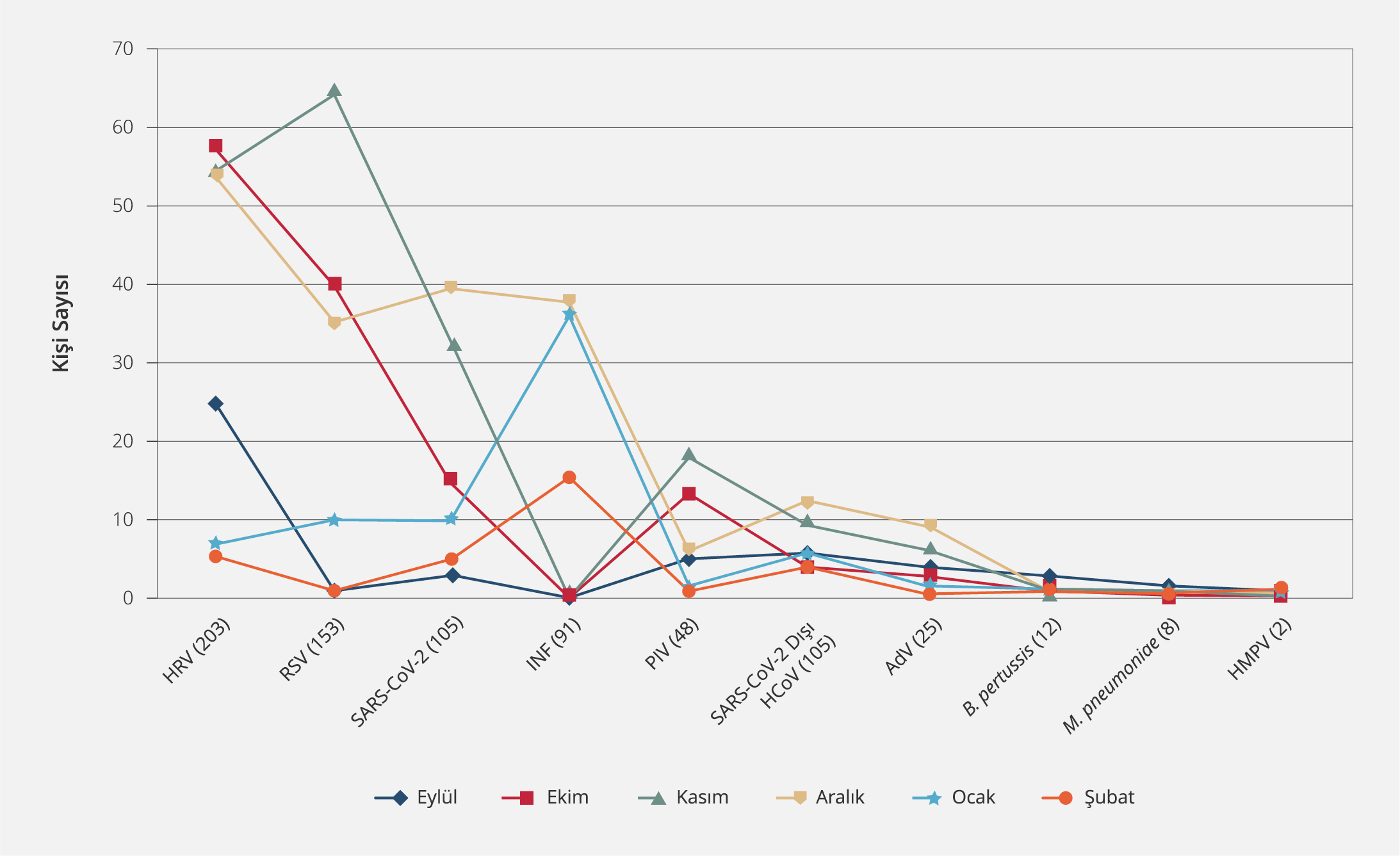
Eylül, Ekim, Aralık aylarında en sık görülen etken HRV iken, Kasım ayında RSV, Ocak ve Şubat ayında ise influenza virusları tespit edilmişti. Etkenlerin aylara göre değişimlerinin istatistiksel olarak anlamlı olduğu belirlendi (p<0.05). Aylara göre görülme sıklıkları değişmeyen etkenler B. pertussis, M. pneumoniae ve HMPV idi (Şekil 2).
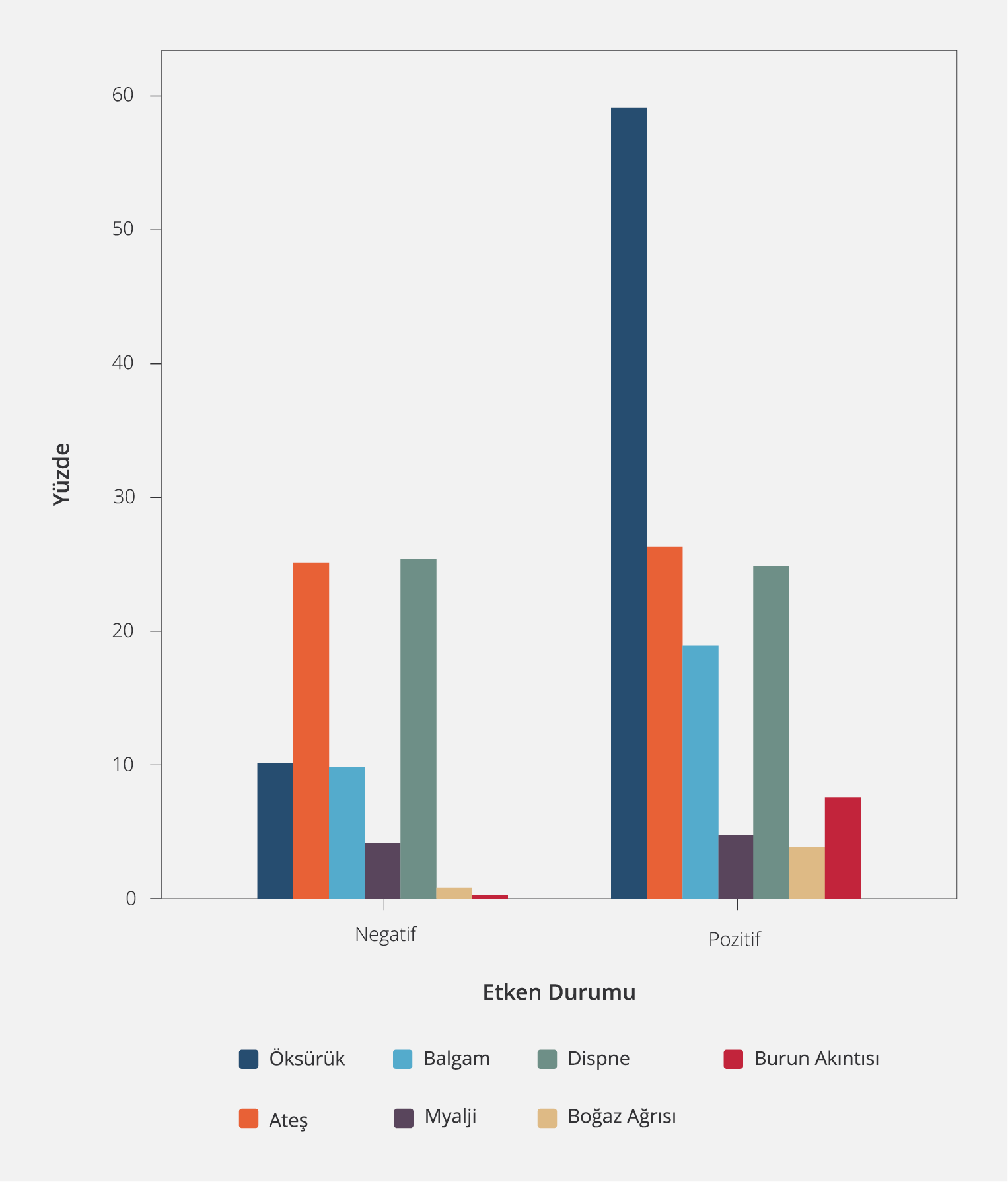
Panel pozitif ve negatif hastaların örnek alımı esnasındaki şikayetleri incelendiğinde, panel pozitif grupta en sık karşılaşılan şikâyet öksürük (%58.85) olup bu hastaların %81.2’sinde en az bir etken pozitif idi. Pozitif hastalar, en belirgin olarak öksürük açısından negatif hastalardan ayrışırken, balgam, boğaz ağrısı ve burun akıntısı da diğer öne çıkan klinik bulgular olarak gözlendi (Şekil 3).
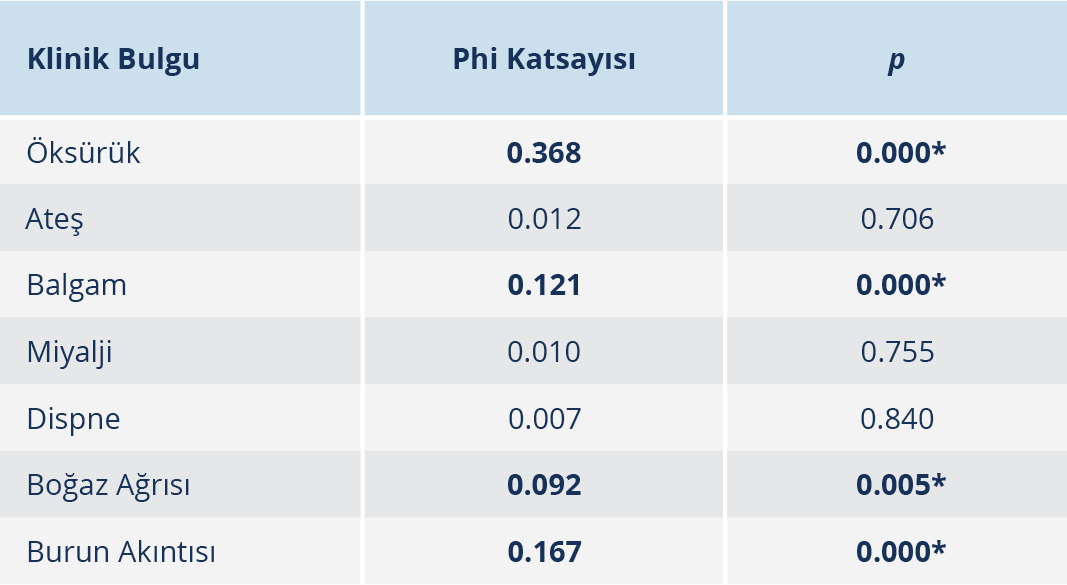
Etken durumu ile klinik bulgular arasındaki ilişki incelendiğinde, sırasıyla öksürük, burun akıntısı, balgam ve boğaz ağrısının istatistiksel olarak anlamlı bir farklılık gösterdiği tespit edildi (p<0.05). Dolayısıyla bu klinik bulguların varlığında, hastaların %95 olasılıkla etken pozitif olduğu söylenebilir (Tablo 2).
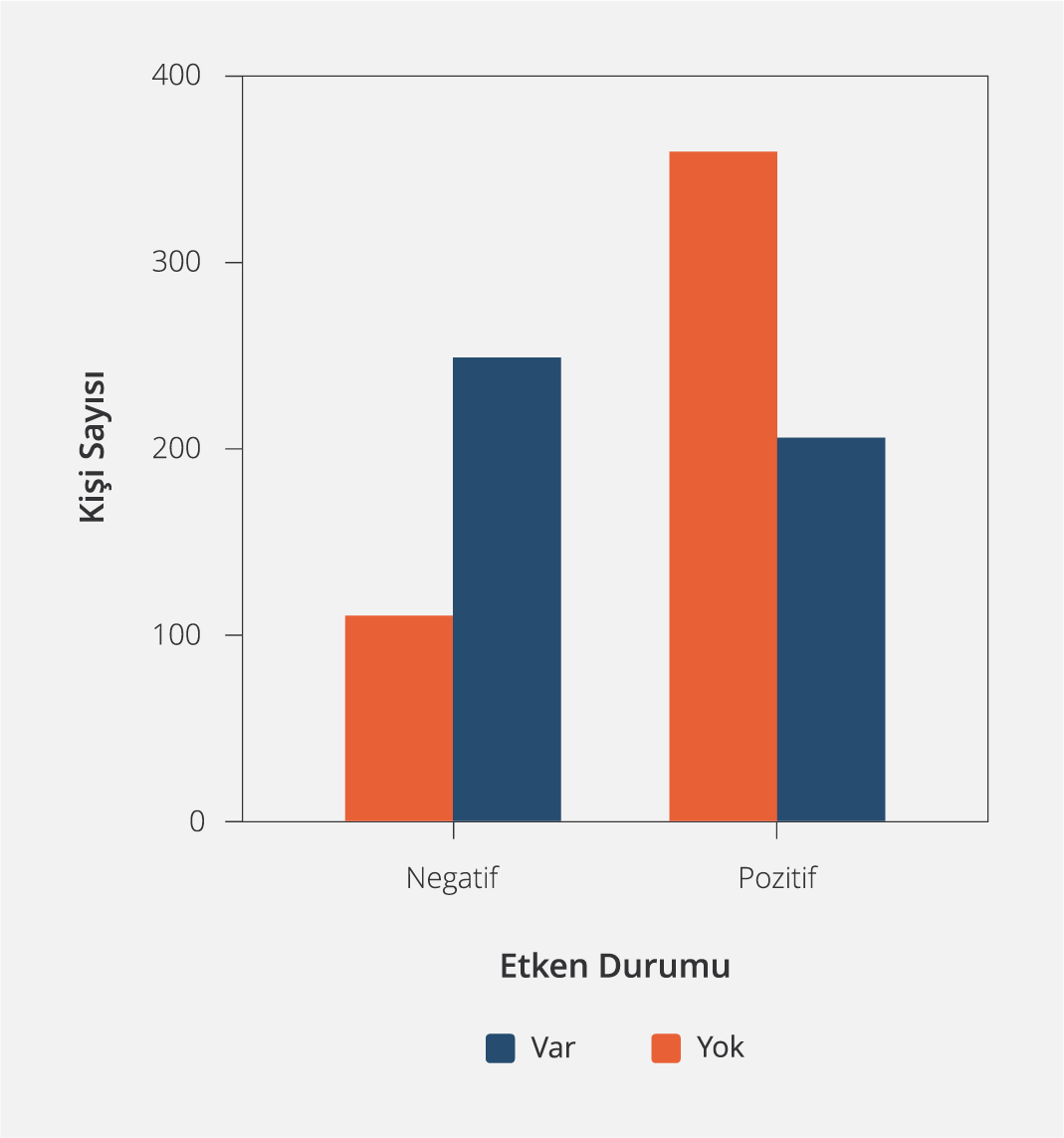
Etken durumu ile ek hastalık varlığı arasındaki ilişki Şekil 4’te sunuldu. Panel negatif grupta ek hastalık varlığı panel pozitif gruba göre daha fazla olup istatistiksel olarak da anlamlı idi (p<0.05). Ek hastalığı bulunan kişilerin %55.2’sinin panel sonucu negatifti. Bu hastaların %80.24’ünde öksürük görülmeyip %35.08’inde de hiç semptom tespit edilmedi. Ayrıca, ek hastalık olarak herhangi bir hematolojik hastalığa sahip kişilerin %61.6’sında panel sonucu negatifti. CRP değeri ve lökosit sayısı açısından panel pozitif ve negatif gruplar arasındaki kesim noktalarını belirlenmek için ROC eğrisinden yararlanıldı; CRP ve lökosit için “area under the curve” (AUC) değerleri sırasıyla 0.571 ve 0.547 idi (Şekil 5). Bu değerler 0.5’e yakın olduğundan güvenilir ve ayırt edici bir kesim noktası belirlenemedi. Negatif ve pozitif hastaların ek hastalık varlığındaki CRP değerlerine ilişkin özet istatistikler Tablo 3’te sunuldu. Negatif ve pozitif hastaların ek hastalık durumuna göre CRP medyan değerleri arasında fark olup olmadığı Mann-Whitney U testi ile analiz edildi. Panel sonucu negatif olup ek hastalığı olan kişilerin CRP medyan değerleri panel sonucu negatif ve ek hastalığı olmayanlara göre daha büyüktü. Benzer şekilde, pozitif ve ek hastalığı bulunan kişilerin CRP medyan değerleri, pozitif ve ek hastalığı olmayan kişilere kıyasla daha yüksek bulundu. Sonuç olarak, CRP değerleri hem pozitif hem negatif olan hasta gruplarında ek hastalık varlığına bağlı olarak anlamlı düzeyde yüksek bulundu (p<0.05).
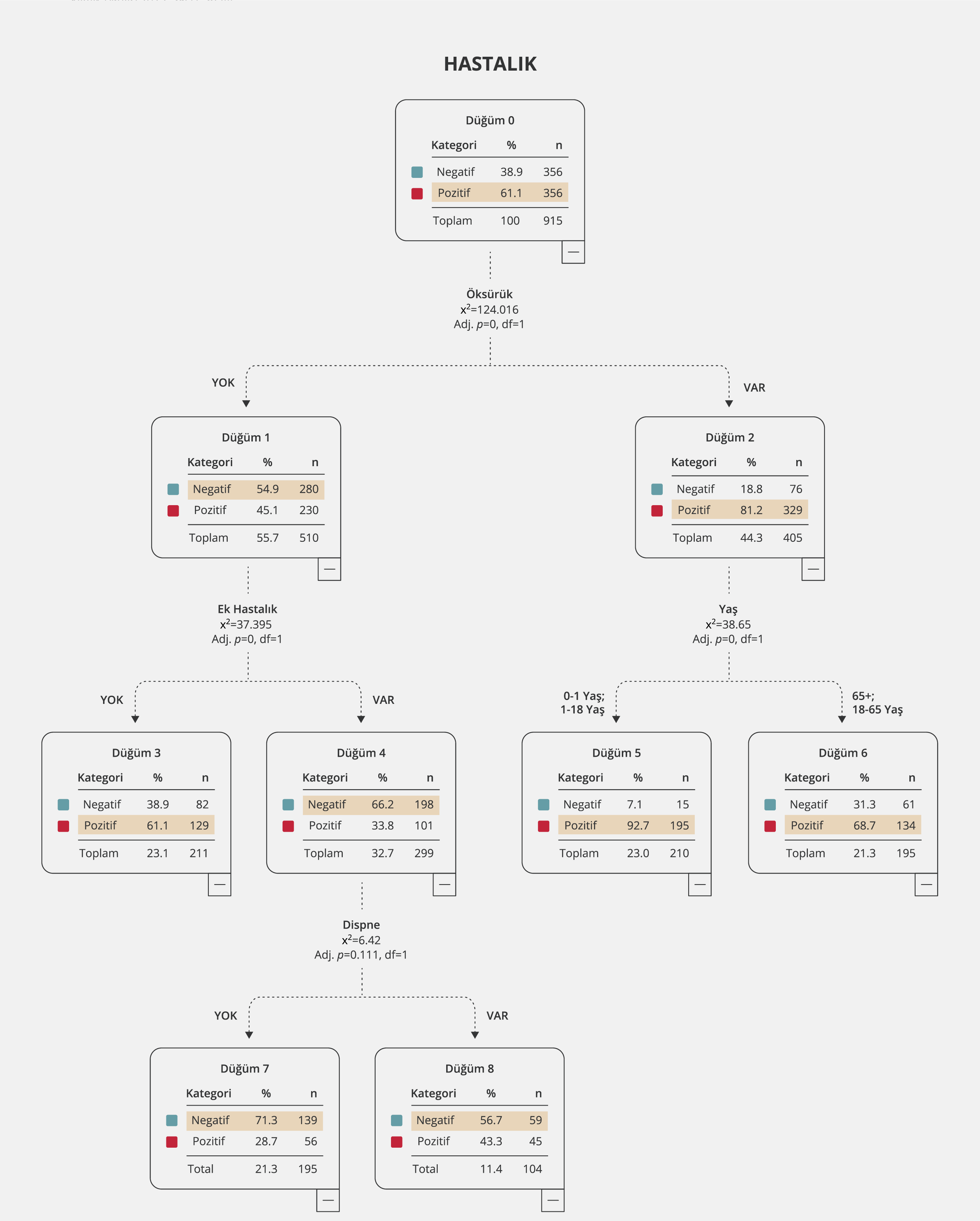
Şekil 6’da sunulan CHAID algoritmasına göre, panel sonucunun pozitif veya negatif olmasında sırasıyla öksürük durumu, yaş, ek hastalık ve dispnenin etkili olduğu gözlendi. Panel pozitif hastalarda öksürük sıklığı, panel negatif gruba kıyasla istatistiksel olarak anlamlı düzeyde yüksek bulundu (p<0.05). Öksürüğü olan kişilerde hastalığın pozitif olma oranı %81.2 olarak tespit edildi; bu noktada, yaş aralıklarının da hastalığın pozitif olma oranlarını etkilediği görüldü. Öksürüğü olup 18 ve daha küçük yaşta olan kişilerde hastalığın pozitif olma oranı %92.9 iken 18’den büyük yaştaki kişiler için bu oran %68.7’ye düşmekteydi. Dolayısıyla öksürük varlığı, yaş aralıklarına göre farklı pozitiflik oranları göstermekle birlikte hastalığın pozitif olmasında oldukça etkilidir.
CHAID algoritmasına göre, ek hastalık varlığı istatistiksel olarak panel negatif grupta daha yaygın idi (p<0.05). Ayrıca, öksürüğü bulunmayan ve ek hastalığı olan kişilerde negatiflik oranının istatistiksel olarak anlamlı olduğu belirlendi (p<0.05). Dispne varlığı açısından ise pozitif ve negatif gruplar arasında istatistiksel olarak anlamlı bir fark tespit edilmemekle birlikte öksürük semptomu olmayan ve ek hastalığı bulunan hastalarda negatiflik oranının istatistiksel olarak anlamlı olduğu tespit edildi (p<0.05). Dispnesi olmayan ve ek hastalığı olan kişilerin %71.3’ünde panel sonucu negatifti. CHAID algoritmasının sınıflama başarısı %72 [Güven aralığı (GA)=%0.68 – %79] olarak, duyarlılık ve özgüllüğü ise sırasıyla %82 ve %56 olarak tespit edildi.
İRDELEME
Solunum yolu infeksiyonları, ağırlıklı olarak çocukluk döneminde görülmekle birlikte, tüm dünyada önemli bir halk sağlığı sorunu olarak önemli bir mortalite ve morbidite nedenidir (10). Etken çoğunlukla viral olmasına rağmen SYİ’ler en çok antibiyotik tedavisi başlanan hastalıkların başında gelmektedir (5,11). Moleküler testler, klinik pratik içerisinde özellikle viral etkenlerin hâkim olduğu etiyolojinin saptanabilmesi açısından önemli katkılar sağlamaktadır.
Solunum yolu infeksiyonları genel olarak viruslardan kaynaklanır ve bunu bakteriyel infeksiyonlar izler. Ancak bu iki etken grubunun neden olduğu semptomlar spesifik değildir ve birbirinden ayırt edilemez. Mevcut tanı yöntemlerinin zamanında ve doğru sonuçları sağlamadaki sınırlılıkları nedeniyle de bu infeksiyonlar genellikle ampirik geniş spektrumlu antibiyotiklerle tedavi edilmektedir (12,13). Günümüzde uygunsuz antibiyotik kullanımı özellikle SYİ’lerde çok yüksektir (5). Bu durum halk sağlığı tehdidi olan antibiyotik direncinin en önemli nedenlerinden biridir (14). Moleküler testlerin antibiyotik kullanımına etkisi ile ilgili farklı sonuçlar veren çalışmalar mevcuttur (15-17). Çalışmamızda, solunum yolu paneli istemi yapılan toplam 915 hastanın test sonuçlarının %61.09’u pozitifti ve pozitif hastaların da %96.6’sında viral bir ya da birden fazla etken saptanmıştı. Viral etkenlerin kısa bir sürede tespit edilmesi, ampirik başlanan ya da başlanması planlanan antibiyotiklerin kullanımına gerek kalmadığını gösterebilir. Diğer yanda, hızlı tanı sayesinde uygun antiviral tedavinin kısa sürede başlanması da mümkün olmaktadır. Ayrıca etkenin hızlı tespiti, uygun olmayan antibiyotik kullanımının önlenmesinin yanı sıra, hastaneye yatan hastalardaki gerekli izolasyon politikalarının uygulanması, bulaşmanın önlenmesi, gerektiği durumlarda temaslı takibi ve gözetiminin yapılması için gerekli stratejilerin uygulanmasını mümkün kılacak ve tamamlayıcı testlere olan ihtiyacın azalmasını da sağlayacaktır (2). Ancak, moleküler testlerin yaygın bir şekilde kullanılması sonucu ortaya çıkacak ekonomik yük de değerlendirilmelidir (13).
Solunum yolu panelinin, etkeni hızlı tespit etmesinin yanı sıra koinfeksiyonları da belirleyebilmesi önemli bir avantajdır. Çalışmamızda, pozitiflik tespit edilen hastaların %21.82’sinde iki veya daha fazla etken birlikte tespit edilmişti. En sık karşılaşılan koinfeksiyon ise HRV-RSV birlikteliği idi. Yapılan çalışmalar, koinfeksiyonların hastalığın şiddetini, bronşiolit ve pnömoni gelişme oranını ve hastaneye yatışların artması gibi olumsuz sonuçlarda rol oynadığını desteklemektedir (18,19). Yapılan bir çalışmada, RSV-HRV ve RSV-PIV koinfeksiyonlarının, bu viruslardan herhangi biriyle gelişen tekil infeksiyonlara kıyasla daha yüksek pnömoni riski oluşturduğuna dair kanıtlar bildirilmiştir (20). Çalışmamızda da RSV-HRV ve RSV-PIV birlikteliği tespit edilen olgular bulunmaktadır. Klasik yöntemlerle tespit edilmesi veya bir klinisyen tarafından öngörülmesi oldukça güç olan fakat ciddi klinik seyirle izleyen bu koinfeksiyonların erken ve doğru tespiti, etkin tedavi ve önlemlerin alınması, klinik sonuçların iyileştirilmesi açısından son derece önemlidir (1). HRV’nin bakteriyel infeksiyonlarla da koinfeksiyon oluşturabildiği ve bu durumun özellikle bağışıklığı baskılanmış hastalarda hastalık şiddetini ve hastaneye yatış oranlarını artırdığı bildirilmiştir (21). Çalışmamızda koinfeksiyona neden olabilecek bakteriyel etkenlerin tamamının panelde bulunmaması nedeniyle çok düşük oranda (%2.14) bakteriyel koinfeksiyon saptandı; ancak bakteriyel etken saptanan hastaların %52.6’sına HRV’nin eşlik ediyor olması dikkate değerdir. Bu nedenle her zaman panel sonuçları klinik bulgular ile birlikte değerlendirilmelidir.
Çalışmamızda, kuzey yarımkürede SYİ’lerin artış gösterdiği sonbahar ve kış ayları için etkenlerin dağılımı incelendi. Eylül, Ekim, Aralık aylarında HRV, Kasım ayında RSV, Ocak ve Şubat ayında ise influenza virusları en sık karşılaşılan etkenlerdi; aylara göre etken dağılımı istatistiksel olarak anlamlı bulundu. Etkenlerin mevsimsel dağılımını bilmek etkene yönelik tedavide, aşılamada, izolasyon önlemlerinde, hasta başı hızlı test uygulamalarında, mini solunum paneli ve bunun gibi daha spesifik testler için doğru zaman aralıklarını seçmede yol gösterici olacaktır (22).
Çalışmamızda solunum yolu paneli sonucu pozitif olan hastalarda en sık bildirilen semptom öksürük olarak tespit edildi; bu hastalarda öksürük, balgam, boğaz ağrısı ve burun akıntısı negatif hastalara kıyasla istatistiksel olarak anlamlı derecede yüksekti. Öksürük, genellikle viral üst solunum yolu infeksiyonlarından kaynaklanmaktadır ve akut öksürük dünya çapında en yaygın SYİ semptomudur (23). Ancak semptoma yönelik tedavi yaklaşımlarının değerlendirildiği bir çalışmada, hastaların %50’sinden fazlasının başvuru nedeninin öksürük olduğu ancak %85’ine uygun olmayan antibiyotik tedavisi uygulandığı bildirilmiştir (24). Çalışmamızda da pozitif saptanan hastalarda en sık bildirilen şikâyetin öksürük olduğu ve bu hastaların %81.2’sinde en az bir etken tespit edildiği belirlendi; tespit edilen etkenlerin tamamına yakını viral etkenlerdi.
Öksürük şikâyeti ile başvuran hastalarda solunum yolu paneli kullanılarak kısa sürede viral bir ya da birden fazla etken tespit edilmesi, antibiyotiklerin uygunsuz kullanımını önleyebilir. Bu tür testler kısa sürede sonuç vermeleri nedeniyle çok fazla tercih edilse de tüm moleküler testlerde olduğu gibi akılcı bir algoritma ile birlikte kullanılmalıdır (25). Bu aşamada, hastaların şikâyetleri ön plana çıkmaktadır. Hastalığın tanısı için anlamlı olan şikâyetlerin kişide saptanması, pozitifliği artırmakta ve akılcı bir kullanım sağlamaktadır. CHAID algoritmasında öksürükten sonraki parametrenin yaş olduğu belirlendi. Öksürüğü olan, ≤18 yaş hastalarda pozitiflik oranı %92.9 olarak hesaplanırken, öksürüğü olmayan hastalarda bu oran %45.1 idi. Ek hastalık varlığı açısından pozitif ve negatif gruplar karşılaştırıldığında, ek hastalığı olan kişilerde negatif sonuç oranı istatistiksel olarak anlamlı derecede yüksekti. Bu durum incelendiğinde, ek hastalığı bulunan ve sonucu negatif olan hastaların %80.24’ünde öksürük olmadığı, %35.08’inde ise hiç şikayet olmamasına rağmen test istemi yapıldığı görüldü. Bu sonuç, hastalardaki ek hastalık varlığının testin akılcı kullanımını olumsuz etkilediğini göstermektedir. Yine CHAID algoritmasına göre ek hastalık varlığında pozitiflik oranı azalırken bu hastalara dispne eşlik ediyorsa oranın eşlik etmeyenlere kıyasla nispeten arttığı tespit edildi. Diğer yanda kanser, kemoterapi ve radyoterapinin SYİ gibi görünen ancak infeksiyöz olmayan pulmoner infiltrasyonlara neden olabileceği bilinmektedir. Böyle durumlarda panelin kullanılması ise SYİ’yi dışlayarak klinisyenin elini güçlendirebilir (26). Çalışmamızda, hematolojik hastalığı olan kişilerin %61.6’sında panel negatif sonuçlanmıştı. Hematolojik hastalığı olup bağışıklık sistemi baskılanmış hastalarda solunum yolu infeksiyonlarının morbidite ve mortalite açısından risk taşıdığı göz önüne alındığında, bu tür testlerin özellikle bu hasta grubu için kullanılması önerilmektedir (27). Çalışmamızda görülen ek hastalık varlığı ile test pozitifliği arasındaki ters ilişki, hastada herhangi bir bulgu yokken bu gruba karşı hassas davranılması nedeniyle testin istenmiş olması ile açıklanabilir. CHAID algoritmasına göre öksürük şikâyeti olmayan ve ek hastalığı olan kişilerde negatifliğin istatistiksel olarak anlamlı bulunması ve ayrıca bu kişilerde dispnenin yokluğunun da negatifliği istatistiksel olarak anlamlı düzeyde etkilemesi klinik bulguların varlığının önemini göstermektedir. Bu durum semptomu olmayan kişilerde testin, bir tarama testi olarak kullanılmaması gerektiğini de göstermektedir. Sendromik testlerin kimlerden istenmesi gerektiğinin tartışıldığı bir çalışmada, kliniğin yol gösterici olması gerektiği ve şiddetli SYİ durumunda maliyetten bağımsız bir şekilde testin istenmesi gerektiği bildirilmiştir (13).
Panel istemi öncesinde elde edilen laboratuvar parametrelerinden faydalanabilmek amacıyla her iki gruptaki hastaların CRP ve lökosit değerleri incelendi. Ancak ön görülebilir bir “cut-off” değeri belirlenemedi. Bu durum etkenlerin tamamına yakınının viral olması ile ilişkilendirildi. Ülkemizde yapılan bir çalışmada, CRP yüksekliği tespit edilen hastaların sadece %42’sinin bir infeksiyon hastalığına sahip olduğu ve infeksiyon hastalığı ile uyumlu semptom varlığının CRP değerine göre tanıda daha önemli olduğu bildirilmiştir (28). CRP değerinin ve lökosit sayısının infeksiyon dışı hastalıklarda da arttığı bilinmektedir. Özellikle CRP inflamasyon belirteci olarak birçok infeksiyöz olmayan hastalıkta da artmaktadır (29-34). Çalışmaya dahil edilen hastaların %49.28’inde ek hastalık olduğu ve bu hastaların %64.5’inde kardiyovasküler hastalık, %23.5’inde akut veya kronik böbrek yetmezliği olduğu tespit edildi. Literatürde, kardiyovasküler hastalık ve böbrek yetmezliği olan kişilerde CRP değerinin anlamlı düzeyde yüksek olduğu çalışmalar mevcuttur (33,34). Çalışmamızda, panel negatif grupta ek hastalık varlığının daha fazla olması, CRP açısından ROC eğrisi analizinde pozitif ve negatif gruplar arasında anlamlı fark bulunmamasının nedenlerden biri olabilir. Ayrıca CRP değerinin hem etken pozitif hem etken negatif hasta gruplarında ek hastalığı olan bireylerde, ek hastalığı olmayanlara göre istatistiksel olarak anlamlı düzeyde yüksek bulunması, CRP değerinin ek hastalık varlığından etkilendiğini göstermektedir (p<0.05). CRP düzeyi ve lökosit sayısının birçok durumdan etkilendiği ve sadece bu değerlere bakılarak solunum yolu paneli istemi yapılmaması gerektiği söylenebilir; mutlaka hastanın şikayetleri sorgulanmalıdır.
Çalışmamızda, panel istemi yapılan hastalar yaş, cinsiyet, klinik durum, CRP düzeyi ve lökosit sayısı, servis ve istem yapılan aylara göre değerlendirildi ve etkenlerin tamamına yakınının viral olduğu tespit edildi. Pozitif ve negatif hastalar arasında cinsiyet, CRP düzeyi ve lökosit sayıları açısından, örneğin gönderildiği bölüme göre anlamlı düzeyde bir fark bulunmazken, tanı algoritmasında öksürük ve yaş pozitiflik yönünde, ek hastalık ise negatiflik yönünde istatistiksel olarak anlamlı bulundu. Bu nedenle, klinik bulgularda öksürük varlığı testin isteminde mutlaka sorgulanmalı ve hastanın yaşı göz önünde bulundurulmalıdır. Ayrıca ek hastalık varlığının klinisyenleri yanıltmaması için semptomlar mutlaka sorgulanmalıdır. Sağlık kuruluşlarında, panellerin yaygın kullanımının bütçe üzerindeki etkisi ve erken tanının sağlayacağı faydalar dikkate alınmalıdır. Bu süreçte, klinisyenler ve mikrobiyologlar iş birliği yaparak hangi hastalar için test istemi yapılacağına karar vermeli ve ortaya çıkabilecek ekonomik yük de göz önünde bulundurularak daha kapsamlı bir istem algoritması oluşturulmalıdır.
Bu çalışma, solunum yolu panelinin uygun olan hastalarda kullanımının önemini vurgulamaktadır. Bulgularımız, viral etkenlerin sıklığının çok yüksek olduğunu göstermektedir. Moleküler testler, duyarlı ve hızlı bir şekilde etkenin virus veya bakteri olduğunu tespit edebilir ve bu şekilde gereksiz antibiyotik kullanımının önüne geçilmesine yardımcı olabilir. Semptomatik hastalarda etken saptama oranı daha yüksek bulunurken, asemptomatik ancak ek hastalığı olan kişilerde pozitiflik oranının düşük olması, bu panelin bir tarama testi olarak kullanılmaması gerektiğini göstermektedir.
Sonuç olarak; çalışmamızda, test pozitifliği ile birlikte en sık görülen semptom öksürük idi. Yaş grupları değerlendirildiğinde ise ≤18 yaş kişilerde pozitiflik oranının anlamlı derecede yüksek olduğu görüldü. Bu nedenle, özellikle erken yaşta antibiyotik başlanmasını önleyerek antibiyotik direncini azaltmak ve testlerin akılcı kullanımını sağlamak için hızlı moleküler testlerin öksürük semptomu bulunan ve 18 yaş altında olan hastalarda kullanımı uygun bir strateji olarak öne çıkmaktadır.
Hasta Onamı
Veriler retrospektif olarak değerlendirildiği için hasta onamı alınmamıştır.
Etik Kurul Kararı
Çalışma için Giresun Eğitim ve Araştırma Hastanesi Bilimsel Araştırmalar Etik Kurulu’ndan 6 Kasım 2023 tarih ve 06.11.2023/10 karar numarasıyla onay alınmıştır.
Danışman Değerlendirmesi
Bağımsız dış danışman
Yazar Katkıları
Fikir/Kavram –M.U., A.M.Ş.; Tasarım – M.U., A.M.Ş.;Denetleme – M.U., A.M.Ş.;Kaynak ve Fon Sağlama – M.U., A.M.Ş.;Malzemeler/Hastalar – M.U., A.M.Ş.;Veri Toplama ve/veya İşleme – M.U., A.M.Ş., E.A.; Analiz ve/veya Yorum – M.U., A.M.Ş., E.A.;Literatür Taraması – M.U., A.M.Ş., E.A.;Makale Yazımı – M.U., A.M.Ş., E.A.;Eleştirel İnceleme –M.U., A.M.Ş., E.A.
Çıkar Çatışması
Yazarlar herhangi bir çıkar çatışması bildirmemiştir.
Finansal Destek
Yazar finansal destek beyan etmemiştir.
Referanslar
- Upadhyay P, Reddy J, Proctor T, et al. Expanded PCR panel testing for identification of respiratory pathogens and coinfections in influenza-like illness. Diagnostics (Basel). 2023;13(12):2014. [CrossRef]
- van Asten SAV, Boers SA, de Groot JDF, Schuurman R, Claas ECJ. Evaluation of the GenmarkePlex® and QIAstat-Dx® respiratory pathogen panels in detecting bacterial targets in lower respiratory tract specimens. BMC Microbiol. 2021;21(1):236. [CrossRef]
- Hong YJ, Jung BK, Kim JK. Epidemiological characterization of respiratory pathogens using the multiplex PCR FilmArray™ Respiratory Panel. Diagnostics (Basel). 2024;14(7):734. [CrossRef]
- Özdemir C, Ergin A. [Validation of Turkishparentalperception on antibioticsscale]. KlimikDerg. 2023;36(1)32-8. Turkish.[CrossRef]
- Piltcher OB, Kosugi EM, Sakano E, et al. How to avoid the inappropriate use of antibiotics in upper respiratory tract infections? A position statement from an expert panel. Braz J Otorhinolaryngol. 2018;84(3):265-79. [CrossRef]
- Loeffelholz MJ, Pong DL, Pyles RB, et al. Comparison of the FilmArray Respiratory Panel and Prodesse real-time PCR assays for detection of respiratory pathogens. J Clin Microbiol. 2011;49(12):4083-8. [CrossRef]
- Leber AL, Lisby JG, Hansen G, et al. Multicenter evaluation of the QIAstat-Dx Respiratory Panel for detection of viruses and bacteria in nasopharyngeal swab specimens. J Clin Microbiol. 2020;58(5):e00155-20. [CrossRef]
- Biggs D, De Ville B,Suen E. A method of choosing multiway partitions for classification and decision trees. JAppl Stat. 2006;18(1):49-62. [CrossRef]
- Ritschard G. CHAID and earlier supervised tree methods. In: McArdle JJ, Ritschard G, editors. Contemporary Issues in Exploratory Data Mining in the Behavioral Sciences. 1st ed. New York: Routledge; 2013. p. 48-74.
- Aydoğan S, Kırca F, Gözalan A, et al. [Viral respiratory tract infection agents detected between years 2019-2021, COVID-19, and co-infections]. Mikrobiyol Bul. 2023;57(4):650-9. Turkish. [CrossRef]
- Rao S, Lamb MM, Moss A, et al. Effect of rapid respiratory virus testing on antibiotic prescribing among children presenting to the emergency department with acute respiratory illness: A randomized clinical trial. JAMA Netw Open. 2021;4(6):e2111836. [CrossRef]
- Grech AK, Foo CT, Paul E, Aung AK, Yu C. Epidemiological trends of respiratory tract pathogens detected via mPCR in Australian adult patients before COVID-19. BMC Infect Dis. 2024;24(1):38. [CrossRef]
- Huang E, Wang Y, Yang N, Shu B, Zhang G, Liu D. A fully automated microfluidic PCR-array system for rapid detection of multiple respiratory tract infection pathogens. Anal Bioanal Chem. 2021;413(7):1787-98. [CrossRef]
- Harris AM, Hicks LA, Qaseem A; High Value Care Task Force of the American College of Physicians and for the Centers for Disease Control and Prevention. Appropriate antibiotic use for acute respiratory tract infection in adults: Advice for high-value care from the American College of Physicians and the Centers for Disease Control and Prevention. Ann Intern Med. 2016;164(6):425-34. [CrossRef]
- Keske Ş, Ergönül Ö, Tutucu F, Karaaslan D, Palaoğlu E, Can F. The rapid diagnosis of viral respiratory tract infections and its impact on antimicrobial stewardship programs. Eur J Clin Microbiol Infect Dis. 2018;37(4):779-83. [CrossRef]
- Moradi T, Bennett N, Shemanski S, Kennedy K, Schlachter A, Boyd S. Use of procalcitonin and a respiratory polymerase chain reaction panel to reduce antibiotic use via an electronic medical record alert. Clin Infect Dis. 2020;71(7):1684-9. [CrossRef]
- Wils J, Saegeman V, Schuermans A. Impact of multiplexed respiratory viral panels on infection control measures and antimicrobial stewardship: a review of the literature. Eur J Clin Microbiol Infect Dis. 2022;41(2):187-202. [CrossRef]
- Essa S, Owayed A, Altawalah H, Khadadah M, Behbehani N, Al-Nakib W. Mixed viral infections circulating in hospitalized patients with respiratory tract infections in kuwait. Adv Virol. 2015;2015:714062. [CrossRef]
- Salar-Gül S, Çiftçi N, Türk-Dağı H, Arslan U. [Investigation of respiratorypathogensresponsibleforcoinfection in COVID-19 patients]. KlimikDerg. 2024;37(2):91-6. Turkish.[CrossRef]
- Yoshida LM, Suzuki M, Nguyen HA, et al. Respiratory syncytial virus: co-infection and paediatric lower respiratory tract infections. Eur Respir J. 2013;42(2):461-9. [CrossRef]
- Esneau C, Duff AC, Bartlett NW. Understanding rhinovirus circulation and impact on illness. Viruses. 2022;14(1):141. [CrossRef]
- Kuşkucu MA, Mete B, Tabak F, Midilli K. [Prevalence and seasonal distribution of respiratory viruses in adults between 2010-2018]. Turk MikrobiyolCemiyDerg. 2020;50(1):21-6. Turkish.[CrossRef]
- Murgia V, Manti S, Licari A, De Filippo M, Ciprandi G, Marseglia GL. Upper respiratory tract infection-associated acute cough and the urge to cough: New insights for clinical practice. Pediatr Allergy Immunol Pulmonol. 2020;33(1):3-11. [CrossRef]
- Morice A, Kardos P. Comprehensive evidence-based review on European antitussives. BMJ Open Respir Res. 2016 Aug 5;3(1):e000137. [CrossRef]
- Şahin AM, Uğur M. [Rational use of molecular methods in the diagnosis of meningitis/encephalitis]. KlimikDerg. 2023;36(4):251-5. Turkish.[CrossRef]
- Anderson EJ. Respiratory infections. In: Stosor V, Zembower TR, editors. Infectious complications in cancer patients, cancer treatment and research. Switzerland: Springer; 2014. p. 203-36.
- Ramanan P, Bryson AL, Binnicker MJ, Pritt BS, Patel R. Syndromic panel-based testing in clinical microbiology. Clin Microbiol Rev. 2017;31(1):e00024-17. [CrossRef]
- Koşar EB, Manavlı B, Dilek O, Çolak G, Demirtürk N. [Evaluation of patients who were consulted to the infectious diseases and clinical microbiology clinic because of high C-reactive protein levels at a university hospital]. KlimikDerg. 2024;37(1):50-3. Turkish.[CrossRef]
- Kushner I, Rzewnicki D, Samols D. What does minor elevation of C-reactive protein signify? Am J Med. 2006;119(2):166.e17-28. [CrossRef]
- Giles JT, Bartlett SJ, Andersen R, Thompson R, Fontaine KR, Bathon JM. Association of body fat with C-reactive protein in rheumatoid arthritis. Arthritis Rheum. 2008;58(9):2632-41. [CrossRef]
- Nadeem R, Hussain T, Sajid H. C reactive protein elevation among children or among mothers’ of children with autism during pregnancy, a review and meta-analysis. BMC Psychiatry. 2020;20(1):251. [CrossRef]
- Gonzalez-Gay MA, Lopez-Diaz MJ, Barros S, et al. Giant cell arteritis: laboratory tests at the time of diagnosis in a series of 240 patients. Medicine (Baltimore). 2005;84(5):277-90. [CrossRef]
- Hage FG. C-reactive protein and hypertension. J Hum Hypertens. 2014;28(7):410-5. [CrossRef]
- Ayar Y, Sayılar EI, Yavuz M, et al. [An enflammatory marker in chronic renal failure patients: Visfatin]. Medical Bulletin of Haseki. 2015;53(3):187-91. Turkish. [CrossRef]